
Жиры в химии - свойства, формула, получение, номенклатура и определение с примерами
Содержание:
Жиры — природные продукты, образующиеся в животных и растительных организмах.
Строение жиров
Основным компонентом жиров являются триглицериды — полные сложные эфиры, образованные глицерином и высшими карбоновыми кислотами.
В природных жирах — растительных и животных — присутствует небольшое количество других веществ (фосфатиды, свободные карбоновые кислоты, витамины, красители).
Свойства жиров
Свойства жиров во многом зависят от строения карбоновых кислот, остатки которых входят в состав три-глицеридов. Схема строения триглицеридов приведена на рисунке 80. Символами 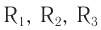
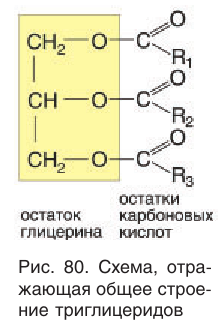
Число атомов углерода в природных карбоновых кислотах, остатки которых входят в состав триглицеридов, всегда четно и колеблется от 4 до 22. Чаще всего встречаются кислоты, которые содержат 16 или 18 атомов углерода (табл. 29). Все эти кислоты имеют неразветвленный углеродный скелет. Молекулы природных ненасыщенных карбоновых кислот имеют цис-конфигурацию (см. табл. 29). В состав триглицеридов в основном входят остатки высших карбоновых кислот, которые называются жирными, потому что впервые эти кислоты были получены из жиров.
Строение жиров было установлено в начале XIX в., когда в процессе их гидролиза получили глицерин и карбоновые кислоты. Впоследствии в середине того же века французский ученый М. Бертло синтезировал жироподобное вещество из глицерина и карбоновых кислот. Французский химик М. Шеврель одним из первых исследовал строение растительных и животных жиров.
Таблица 29. Представители высших жирных карбоновых кислот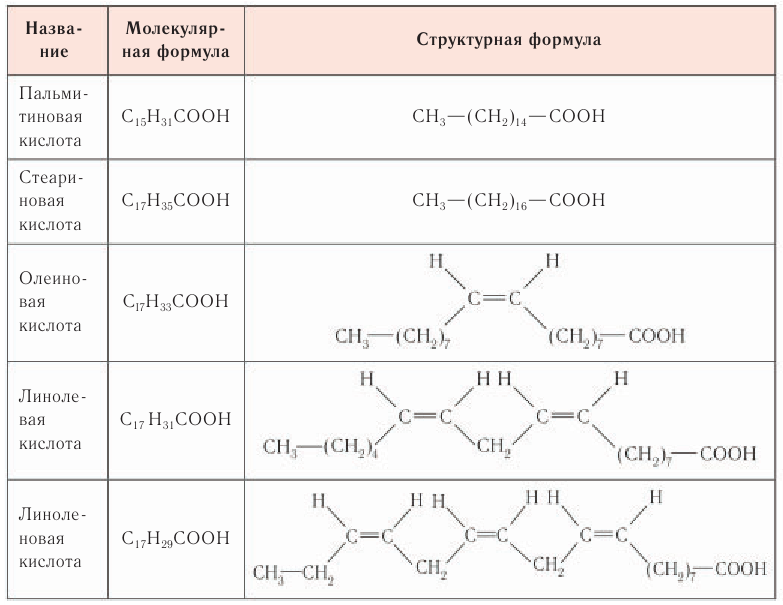
В жирах наиболее часто встречаются остатки таких высших насыщенных кислот, как пальмитиновая, стеариновая, и высших в разной степени ненасыщенных кислот — олеиновой, линолевой, линоленовой.
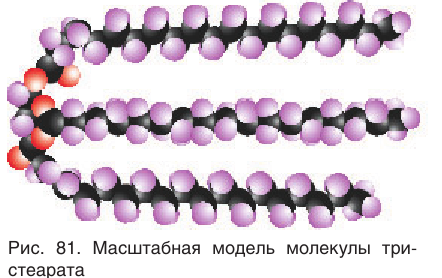
Модель молекулы тристеарата показана на рисунке 81.
В состав некоторых жиров входят триглицериды, содержащие остатки низших кислот. Например, в сливочном масле содержится в небольшом количестве триглицерид масляной кислоты.
Физические свойства жиров
Природные жиры бывают твердые и жидкие, последние называют маслами. Агрегатное состояние жиров зависит от их состава. Если в триглицеридах преобладают остатки насыщенных кислот, то жиры твердые, а если преобладают остатки ненасыщенных кислот, то жиры жидкие. Животные жиры, как правило, твердые, а растительные — жидкие. В таблице 30 приведено содержание карбоновых кислот (в виде остатков) в некоторых жирах.
Таблица 30. Содержание карбоновых кислот (в виде остатков) в составе жиров (% по массе)
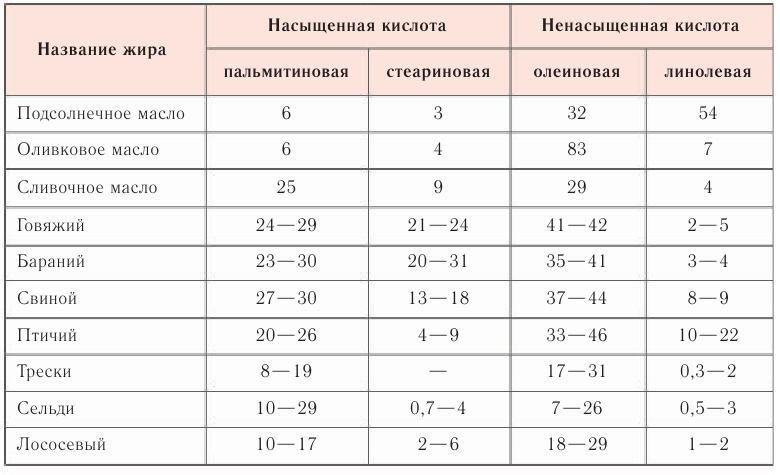
Плотность жиров меньше, чем воды, и в ней они не растворимы. Но они хорошо растворяются в органических растворителях: бензине, бензоле, дихлорэтане, частично в этаноле. Свойство жиров растворяться в органических растворителях используется для очистки одежды от жирных пятен.
Природные жиры представляют собой смеси индивидуальных веществ, поэтому они не имеют четкой температуры плавления, а плавятся в определенном интервале температур. Температура плавления жиров зависит от содержания в них остатков насыщенных кислот и длины углеводородной цепи. С уменьшением содержания остатков насыщенных кислот температура плавления жиров понижается, они становятся легкоплавкими.
Твердые жиры содержатся в жировых тканях наземных млекопитающих и птиц, а жидкие — в тканях морских млекопитающих и рыб, в костях и копытах животных, а также в семенах и плодах растений.
Химические свойства жиров
Для триглицеридов, как и для любых сложных эфиров, характерна реакция гидролиза. Гидролиз происходит под действием воды в присутствии кислот или щелочей.
1) Гидролиз кислотный. В результате кислотного гидролиза образуются глицерин и смесь жирных кислот:
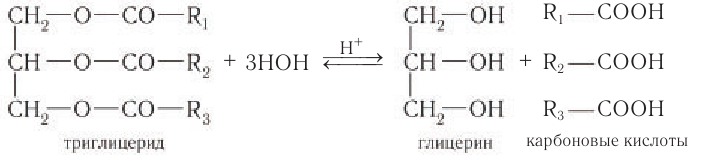
2) Гидролиз щелочной. При щелочном гидролизе образуются глицерин и соли насыщенных жирных кислот, называемые мылами:
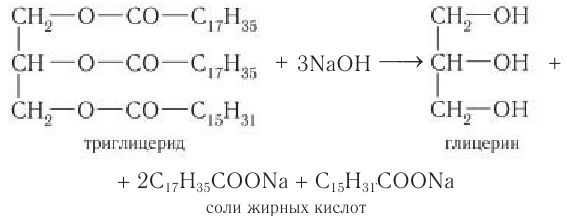
3) Окисление. Жиры при длительном хранении под действием кислорода воздуха, влаги, света, тепла приобретают неприятный запах и вкус. Этот процесс называется химическим прогорканием. Неприятный запах и вкус обусловлены появлением в жирах продуктов их окисления: свободных жирных кислот, альдегидов, гидроксикислот.
4) Гидрирование жидких жиров. Для жидких жиров, триглицериды которых содержат остатки ненасыщенных карбоновых кислот, характерны все реакции ненасыщенных соединений. Они обесцвечивают раствор перманганата калия (в чем вы убедитесь, выполнив лабораторный опыт), вступают в реакцию присоединения, взаимодействуя с галогенами и водородом. Процесс присоединения водорода называют гидрированием.
Под действием водорода остатки ненасыщенных карбоновых кислот переходят в остатки насыщенных кислот, а жиры из жидких превращаются в твердые:
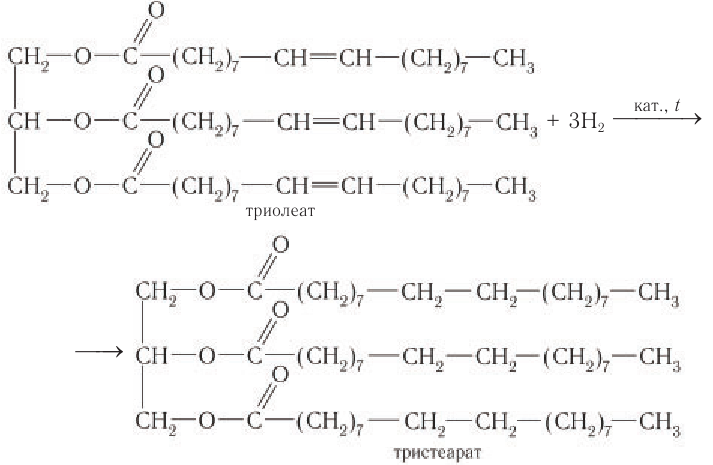
Впервые метод получения твердых жиров из жидких (масел) в процессе гидрирования был разработан русским химиком С. А. Фокиным.
Гидрирование жидких жиров имеет большое промышленное значение, потому что получаемый при этом твердый жир сохраняется значительно дольше и может быть использован для получения мыла, глицерина, стеарина.
Жиры как питательные вещества
Жиры как питательные вещества являются важной составляющей частью пищи человека и животных. В организме они в процессе гидролиза расщепляются на глицерин и карбоновые кислоты. Затем эти продукты гидролиза используются для синтеза специфических для данного организма жиров. Кроме того, жиры — поставщики необходимых ненасыщенных кислот, некоторые из них в организме человека не синтезируются.
Жиры представляют собой один из основных источников энергии для живых организмов. В процессе расщепления жиров выделяется в два раза больше энергии, чем при расщеплении углеводов. Это важная информация при составлении рациона питания. Сведения о содержании жиров в некоторых пищевых продуктах приведены в таблице 31.
Таблица 31. Содержание жиров (в граммах) в некоторых пищевых продуктах (в среднем на 100 г пищевого продукта)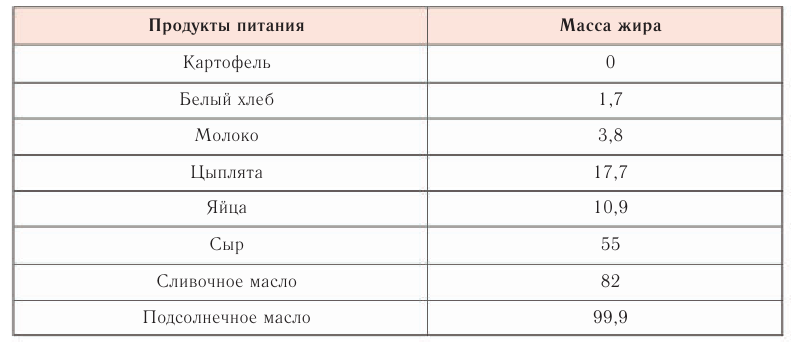
Вы знаете, что маслами называются жиры, которые при комнатной температуре находятся в жидком состоянии. Эти масла представляют собой сложные эфиры глицерина и жирных кислот. Понятие «масла» используется также по отношению к некоторым веществам, которые не являются продуктами питания.
Существуют минеральные масла. Их получают из каменного угля, нефти, они состоят из углеводородов. Примером такого масла является знакомое вам вазелиновое масло. Известны также такие масла, как эфирные. Это летучие вещества с характерным запахом, извлекаемые из растений. По химическому составу они являются смесями углеводородов, спиртов, сложных эфиров или их простых производных. К таким маслам относятся коричное, гвоздичное, ментоловое, миндальное масла и т. д. Эти масла применяются в производстве косметических средств, фармакологии, для получения олифы.
Жиры представляют собой смесь триглицеридов — полных сложных эфиров глицерина и высших карбоновых кислот.
Для жиров характерна реакция гидролиза. Жидкие жиры при гидрировании превращаются в твердые жиры.
Жиры являются ценным пищевым энергетическим продуктом, обеспечивающим нормальное функционирование организма человека.
Мыла и синтетические моющие средства
Мыла, растворимые в воде натриевые и калиевые соли высших жирных кислот — пальмитиновой 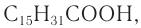 стеариновой
стеариновой 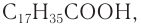 олеиновой
олеиновой 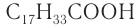 — относятся к веществам, обладающим моющими свойствами. Моющие свойства рассматриваются как способность веществ и их растворов удалять с отмываемой поверхности тканей, изделий и др. прилипшие частицы грязи, жира и переводить их во взвешенное состояние в виде эмульсий и суспензий. Моющие свойства веществ обусловлены строением их молекул. Натриевые и калиевые соли высших карбоновых кислот представляют собой молекулы, в составе которых присутствуют фрагменты с противоположными свойствами по отношению к воде: длинный алкильный гидрофобный фрагмент (не растворимый в воде, а растворимый в жирах и других малополярных веществах) и ионизируемая группа, сообщающая молекуле гидрофильные свойства:
— относятся к веществам, обладающим моющими свойствами. Моющие свойства рассматриваются как способность веществ и их растворов удалять с отмываемой поверхности тканей, изделий и др. прилипшие частицы грязи, жира и переводить их во взвешенное состояние в виде эмульсий и суспензий. Моющие свойства веществ обусловлены строением их молекул. Натриевые и калиевые соли высших карбоновых кислот представляют собой молекулы, в составе которых присутствуют фрагменты с противоположными свойствами по отношению к воде: длинный алкильный гидрофобный фрагмент (не растворимый в воде, а растворимый в жирах и других малополярных веществах) и ионизируемая группа, сообщающая молекуле гидрофильные свойства:
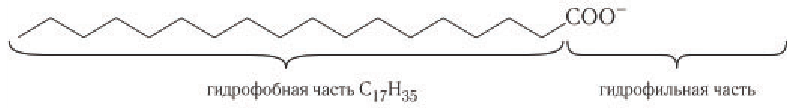
Такие молекулы характерны для поверхностно-активных веществ (ПАВ), т. е. веществ, понижающих поверхностное натяжение на границе раздела двух жидкостей или жидкости и газа.
Дешевые сорта мыла, например хозяйственное мыло, практически полностью состоят из натриевой соли стеариновой кислоты 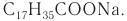 В состав различных сортов туалетного мыла, кроме стеарата натрия, входят соли пальмитиновой кислоты
В состав различных сортов туалетного мыла, кроме стеарата натрия, входят соли пальмитиновой кислоты 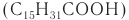 и соли лауриновой кислоты
и соли лауриновой кислоты 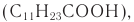 которые получают гидролизом сложных эфиров из плодов масляничной пальмы. В готовом продукте содержатся глицерин (смягчающее вещество), различные наполнители, красители, регуляторы кислотности среды (лимонная кислота) и др.
которые получают гидролизом сложных эфиров из плодов масляничной пальмы. В готовом продукте содержатся глицерин (смягчающее вещество), различные наполнители, красители, регуляторы кислотности среды (лимонная кислота) и др.
При растворении в воде мыла гидрофобная часть молекул натриевых или калиевых солей высших жирных кислот, обладающих поверхностной активностью в отношении неполярной фазы (в данном случае воздуха), выталкиваются из полярной среды (из воды). В этом случае в растворе мыла на границе с воздухом образуется адсорбционный слой с гидрофобными фрагментами молекул, ориентированными в сторону воздуха (рис. 82, а). Число молекул ПАВ в поверхностном слое воды намного больше, чем в растворе, в силу этого ПАВ снижают поверхностное натяжение воды на границе с воздухом. А это приводит к увеличению смачивающей способности воды и увеличению моющих действий моющего средства. Так, мыла понижают в два раза поверхностное натяжение воды, благодаря этому мыльная вода проникает в мельчайшие поры загрязненной поверхности ткани.
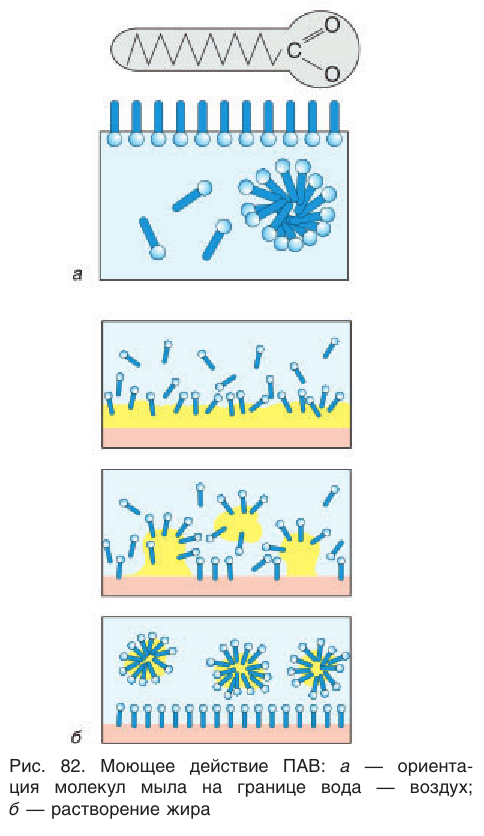
Рассмотрим кратко, как проявляется очищающий эффект мыла в растворе воды и происходит удаление жира с поверхности ткани. Неполярные (гидрофобные) концы молекул стеаратов калия и натрия растворяются в каплях жира, а полярные карбоксилатанионы остаются в водном растворе (рис. 82, б). В результате отталкивания одноименных зарядов на поверхности капли масла она разбивается на мельчайшие частицы. Такие частицы, окруженные большим числом стеаратионов, приобретают свойства полианионов и, как следствие, растворимость в воде с образованием устойчивой эмульсии жира в воде. Мыла являются хорошими пенообразователями. Пене принадлежит важная роль в процессе стирки, так как загрязненные частицы прилипают к ее пузырькам и легко удаляются из раствора.
При использовании мыла как моющего средства в жесткой воде, содержащей ионы кальция и магния, его моющая способность уменьшается. Это объясняется тем, что в растворе образуются нерастворимые кальциевые или магниевые соли высокомолекулярных жирных кислот (рис. 83):
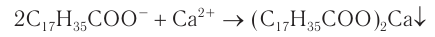
К мылам относят не только натриевые и калиевые соли высших жирных кислот, обладающие моющим действием, но и соли высших жирных карбоновых кислот других металлов 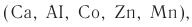 не обладающие моющим действием. Эти соли используют для некоторых промышленных целей. Кобальтовые, свинцовые, марганцевые мыла, растворимые в маслах, применяют в качестве важной составляющей масляных красок. Для изготовления брезента используют алюминиевое мыло, обрабатывая им плотную ткань. Такую смазку, как солидол, получают из нефтяных масел, добавляя в них кальциевое мыло.
не обладающие моющим действием. Эти соли используют для некоторых промышленных целей. Кобальтовые, свинцовые, марганцевые мыла, растворимые в маслах, применяют в качестве важной составляющей масляных красок. Для изготовления брезента используют алюминиевое мыло, обрабатывая им плотную ткань. Такую смазку, как солидол, получают из нефтяных масел, добавляя в них кальциевое мыло.

Синтетические моющие средства
Моющими свойствами обладают синтетические алкил- и арилсульфонаты, представляющие собой натриевые соли органических сульфокислот или монозамещенных сложных эфиров серной кислоты. Их называют детергентами или синтетическими моющими средствами (CMC). Среди веществ этих классов наиболее распространены додецилбензосульфонат натрия и лаурилсульфат натрия:
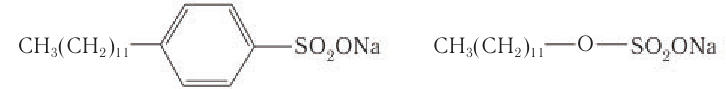
Формулы веществ, относящихся к CMC, приведены в ознакомительном плане и не требуют запоминания.
Синтетические моющие средства так же, как и мыла, обладают поверхностно-активными свойствами, так как в составе их молекул содержатся гидрофобные и гидрофильные группы:
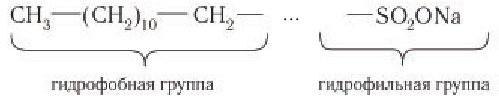
Процесс очищения загрязненной ткани (кожа, поверхность детали и др.) водным раствором CMC протекает так же, как и мылами. Молекулы CMC ориентируются так, что их гидрофильная часть оказывается обращенной к воде, а гидрофобная — к частичке жира. В результате все частички жира оказываются окруженными молекулами CMC. Взаимодействие между отдельными каплями жира ослабляется, и они переходят с загрязненной поверхности в раствор.
CMC как моющие средства имеют ряд преимуществ перед мылами. 11роцесс ценообразования и моющие действия CMC значительно выше, чем мыла, в чем вы сможете убедиться при выполнении соответствующего лабораторного опыта. Синтетические моющие средства сохраняют свои моющие свойства, в отличие от мыла, даже в жесткой воде, так как их кальциевые и магниевые соли, образующиеся в жесткой воде, являются растворимыми веществами. В отличие от растворов мыла, соли которых подвергаются частично гидролизу (поэтому их растворы имеют щелочную среду), соли CMC не подвергаются гидролизу, и их растворы имеют нейтральную среду (рис. 84). В результате CMC можно использовать для стирки изделий из любых тканей.
В состав обычных стиральных порошков, помимо натриевых солей органических сульфокислот и монозамещенных сложных эфиров серной кислоты (CMC), обладающих моющими свойствами и составляющих их основную часть, входят различные добавки. Например, в состав стиральных порошков вводят антиосадители, которые препятствуют обратному осаждению загрязнений на ткани; ферменты, ускоряющие удаление некоторых загрязнителей (пятна от крови, соков); вещества для умягчения воды; парфюмерные отдушки, придающие белью приятный запах, и др.
К моющим средствам относят мыла и синтетические моющие средства (CMC).
Моющие средства являются поверхностно-активными веществами; они содержат в составе молекул две противоположные по свойствам группы: полярную (гидрофильную) и неполярную (гидрофобную), которые обусловливают их моющее действие.
Синтетические моющие средства, в отличие от мыла, сохраняют моющие свойства в жесткой воде.
| Рекомендую подробно изучить предметы: |
| Ещё лекции с примерами решения и объяснением: |