
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Запишите выражение для константы равновесия для заданного уравнения реакции 2А(г) + В(г) = = 3С(г)
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
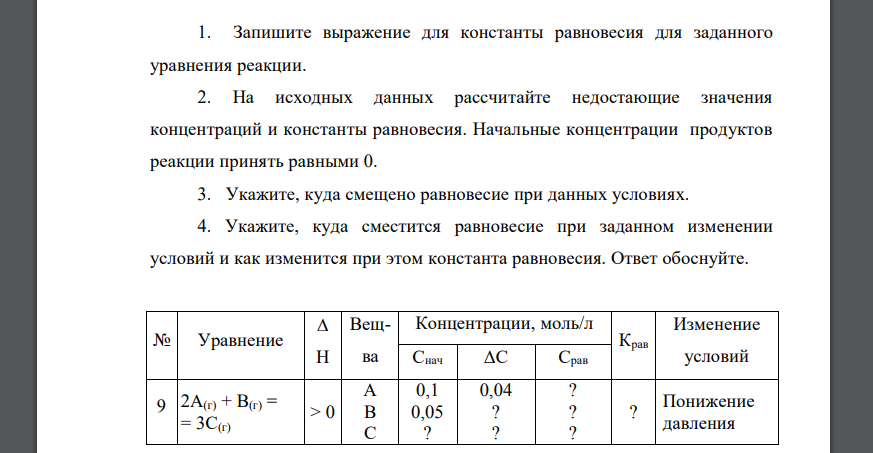
Запишите выражение для константы равновесия для заданного уравнения реакции. 2. На исходных данных рассчитайте недостающие значения концентраций и константы равновесия. Начальные концентрации продуктов реакции принять равными 0. 3. Укажите, куда смещено равновесие при данных условиях. 4. Укажите, куда сместится равновесие при заданном изменении условий и как изменится при этом константа равновесия. Ответ обоснуйте. № Уравнение Н Вещва Концентрации, моль/л Крав Изменение Снач ΔС Срав условий 9 2А(г) + В(г) = = 3С(г) > 0 А В С 0,1 0,05 ? 0,04 ? ? ? ? ? ? Понижение давления
Решение:
Запишем выражение для константы равновесия: 2. Рассчитаем недостающие значения концентрация и константу равновесия. Вещ-ва Концентрации Из условия известно, что в реакцию вступило вещества. Составим пропорцию и определим, сколько моль вещества В вступило в реакцию: Составим пропорцию и определим, сколько моль вещества С образовалось в результате реакции. 2 Рассчитаем равновесные концентрации веществ: Рассчитаем константу равновесия: 3. Поскольку Кравн то равновесие смещено вправо, в сторону прямой реакции. 4. По принципе Ле-Шателье, при понижении давления химическое равновесие смещается в сторону реакции, которая протекает с увеличением количества газообразных веществ. Данная реакция протекает без изменения количеств газообразных веществ (из 3 моль газов образуется 3 моль газов), поэтому понижение давления не смещает химическое равновесие.

- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта 2B(т) + 3Cl2(г) = 2BCl3(г) Сl2 0,9 BCl3
- Приведите уравнения реакций количественного определения прокаина гидрохлорида (новокаина) (Мr 272,78) методом нитритометрии. Укажите индикатор
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию. Железное изделие + анодное покрытие
- Проставьте степени окисления элементов в исходных веществах и продуктах реакции Na2SO3 + KMnO4 + KOH = Na2SO4 + K2MnO4 + H2O K2MnO4 Mn

