
Задания а и б приведены для одного и того же процесса. В задании «а», пользуясь справочными данными, следует вычислить константу равновесия при 298,15 К. CH4(г) + 2F2(г) = 2HF(г) + CH2F2(г)
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16852 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Задания а и б приведены для одного и того же процесса. В задании «а», пользуясь справочными данными, следует вычислить константу равновесия при 298,15 К. CH4(г) + 2F2(г) = 2HF(г) + CH2F2(г) Б) Вычислить начальные концентрации CH4 и F2, если известно, что равновесные концентрации CH4, F2, CH2F2, HF при некоторой температуре равны соответственно 1 моль/л; 2 моль/л; 0,5 моль/л; 1 моль/л, а начальные концентрации CH2F2 и HF равны нулю.
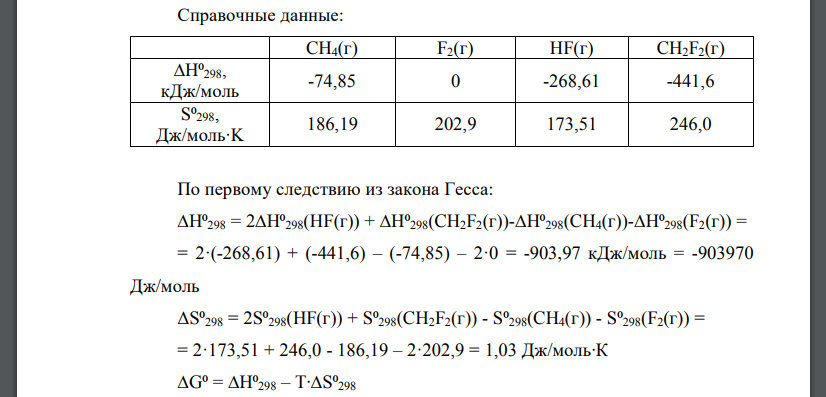
Решение: А) Справочные данные: По первому следствию из закона Гесса: В ходе реакции образовалось и 0. По уравнению реакции видим, что для этого потребовалось и . Тогда начальные концентрации равны: Ответ:

Похожие готовые решения по химии:
- Вычислите концентрацию ионов Clв 0,03 М растворе BaCl2. Дано: С(BaCl2) = 0,03 моль/л
- Константы ступенчатой диссоциации сероводородной кислоты К1 и К2 равны соответственно 6·10-8 и 1·10-13. Определите концентрации ионов H + , HS- и S 2- в 0,05 М растворе H2S.
- Вычислить концентрацию ионов NO3 - в 0,02 М растворе Al(NO3)3. Дано: С(Al(NO3)3)=0,02 моль/л
- Константы ступенчатой диссоциации угольной кислоты К1 и К2 равны соответственно 4,5·10-7 и 4,7·10-11. Определите концентрации Н+ , НСО3 - и СО3 2- в 0,01 М растворе Н2СО3
- До какого объема надо упарить 500 мл 1 М раствора NaNO3, чтобы получить 20 масс % раствор NaNO3 (плотность 1,143 г/мл)? Вычислите молярную концентрацию, титр и моляльность полученного раствора
- Напишите уравнения реакций. Отметьте реакцию диспропорционирования и внутримолекулярного окисления-восстановления. Подтвердите расчетом возможность протекания реакций
- Укажите число связей в молекуле Be2Cl4, образованных по донорноакцепторному механизму. Б. Изобразите схемы перекрывания орбиталей при образовании σ- и πсвязей в молекулах
- Какой тип гибридизации валентных орбиталей атома А отвечает квадратному расположению связей в молекуле, имеющей общую формулу АХ4. Б. Изобразите схемы перекрывания орбиталей при образовании σ- и πсвязей в молекулах
- Какой тип гибридизации валентных орбиталей атома А отвечает квадратному расположению связей в молекуле, имеющей общую формулу АХ4. Б. Изобразите схемы перекрывания орбиталей при образовании σ- и πсвяз
- Укажите число связей в молекуле Be2Cl4, образованных по донорноакцепторному механизму. Б. Изобразите схемы перекрывания орбиталей при образовании σ- и πсвязей в молекулах
- Константы ступенчатой диссоциации сероводородной кислоты К1 и К2 равны соответственно 6·10-8 и 1·10-13. Определите концентрации ионов H + , HS- и S 2- в 0,05 М растворе H2S.
- Вычислите концентрацию ионов Clв 0,03 М растворе BaCl2. Дано: С(BaCl2) = 0,03 моль/л

