
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Вычислите степень диссоциации уксусной кислоты в растворе с концентрацией равной 6,71·10-4 моль/л, а также рН раствора
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16786 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
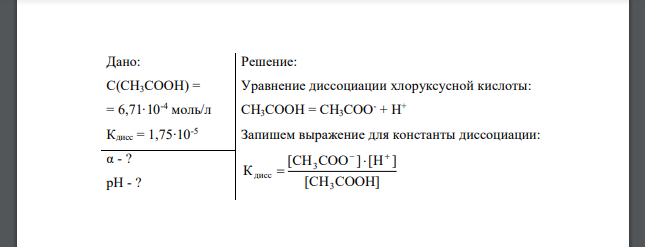
Вычислите степень диссоциации уксусной кислоты в растворе с концентрацией равной 6,71·10-4 моль/л, а также рН раствора. Константа кислотной диссоциации СН3СООН равна 1,75·10-5 . Дано: C(CH3COOH) = = 6,71∙10-4 моль/л Кдисс = 1,75∙10-5
Решение: Уравнение диссоциации хлоруксусной кислоты: Запишем выражение для константы диссоциации: Т.к. и диссоциация протекает в незначительной степени, т.е. , получаем Выразим и рассчитаем концентрацию ионов водорода в растворе: раствора равен: Рассчитаем степень диссоциации: Ответ: 3,97; 16 %
- Задана двумерная дискретная величина: 𝜉1 𝜉2 3 4 0 0,2 0,1 1 0,3 0,3 2 0,04 0,06 Найти дисперсию
- Для определения средней урожайности пшеницы в каждом из десяти хозяйств района была определена урожайность на 100 га в каждом из них. Для
- В химической реакции Na2S2O3 + 2HCl = 2NaCl + S + SO2 + H2O исходная концентрация реагирующих веществ
- Из генеральной совокупности извлечена выборка xi [11, 14) [14, 17) [17, 20) [20, 23) [23, 26) [26, 29) [29, 32] ni 4 10 21 27 22 11 5 Построить

