
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Приведите уравнения реакций количественного определения изониазида (Mr 137,14) методом
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16977 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Приведите уравнения реакций количественного определения изониазида (Mr 137,14) методом йодиметрии. а. Рассчитайте молярную массу эквивалента, титр по определяемому веществу, объем 0,1 моль/л раствора натрия тиосульфата (К=1,02), который пойдет на титрование избытка 0,1 моль/л (УЧ 1/2 I2) раствора йода (К=1,00), добавленного к навеске изониазида массой 0,1024 г в количестве 50,0 мл. На контрольный опыт пошло 49,5 мл 0,1 моль/л раствора натрия тиосульфата. б. Рассчитайте содержание изониазида в анализируемом образце (%) , если на титрование избытка 0,1 моль/л (УЧ 1/2 I2) раствора йода (К=1,01), добавленного в количестве 50,0 мл к навеске массой 0,1078 г, затрачено 19,2 мл 0,1 моль/л раствора натрия тиосульфата (К=0,99), в контрольном опыте – 51,0 мл того же титранта.
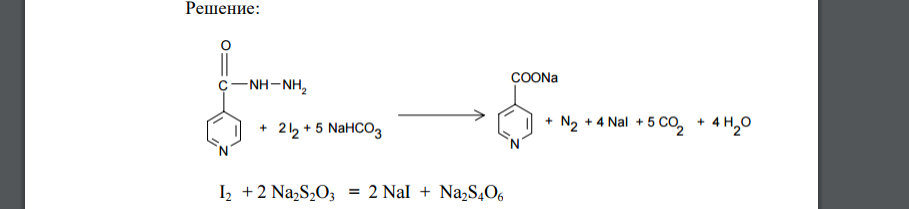
Решение:
А) fэ(изониазид) = 1/4 Содержание изониазида в навеске.
Ответ: 19,64 мл; 100,14 %.

- Приведите уравнения реакций количественного определения хинина гидрохлорида
- Напишите схемы реакций получения дипептидов: а) аланилгистидина; б) фенилаланилтриптофана; в) фенилаланилтирозина.
- Вязкость керосина при 20 °С равна 1,8*10-3 Па·с, а вязкость воды при тех же условиях - 1,005*10-3 Па·с (Н·с/м2 ). Определите плотность керосина, если известно, что время истечения керосина
- Оцените качество раствора цианокобаламина для иньекций по 100 мкг согласно требованиям ФС (цианокобаламина должно быть 0,09 - 0,11 мг/мл), если оптическая

