
Приведите уравнения реакций количественного определения этаминал-натрия (Mr 248,26) методом ацидиметрии (ФС). Укажите
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16970 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
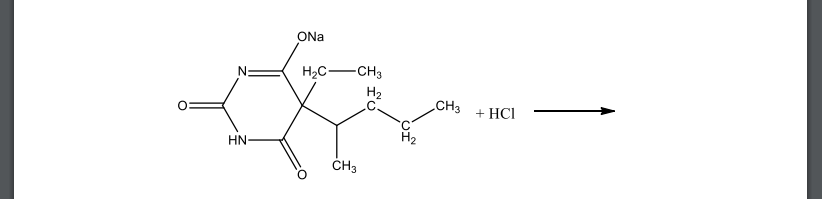
Приведите уравнения реакций количественного определения этаминал-натрия (Mr 248,26) методом ацидиметрии (ФС). Укажите индикатор (название, формулу, переход окраски в конечной точке титрования). Рассчитайте содержание этаминал-натрия в пересчете на сухое вещество (%), если на титрование навески массой 0,5024 г пошло 19,9 мл 0,1 моль/л раствора хлористоводородной кислоты (К=0,98). При расчете учтите содержание в этаминал-натрии свободной щелочи (Mr NaOH 40,0), которое составило 0,3%. Потеря в массе при высушивании этаминал-натрия 4,5%.
Решение:
Уравнение реакции: Определим объем титранта, пошедший на титрование Содержание этаминал-натрия в пересчете на сухое вещество: . Ответ:

- Приведите уравнения реакций количественного определения хинина сульфата (Mr [Хинин]2·H2SO4·2H2O 783,0; Mr H2O 18,0) методом неводного титрования
- Проанализируйте уравнение G = H - TS и укажите, как зависит G от температуры, если а) S < 0, б) S > 0, в) S = 0 Укажите критерий протекания самопроизвольных
- Приведите уравнения реакций количественного определения хлоралгидрата (М = 165,40 г/моль) по методике ГФ, индикатор (название, формулу, переход окраски в конечной
- Приведите уравнения реакций количественного определения бензилпенициллина новокаиновой соли методом иодиметрии. Рассчитайте

