
По зависимости давления насыщенного пара от температуры и плотности данного вещества А с молекулярной массой М в твердом и жидком состояниях
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16722 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
По зависимости давления насыщенного пара от температуры и плотности данного вещества А с молекулярной массой М в твердом и жидком состояниях в тройной точке (тр.т): 19. постройте график зависимости давления насыщенного пара от температуры, укажите линию возгонки, линию плавления, линию испарения; 20. постройте график зависимости определите по графику координаты тройной точки; 22. рассчитайте среднюю теплоту испарения и возгонки; 23. определите теплоту плавления вещества при температуре тройной точки; 24. вычислите для процесса плавления при температуре тройной точки; 25. вычислите температуру плавления вещества при давлении Р Па; 26. вычислите изменение энтропии, энергий Гиббса и Гельмгольца, энтальпии и внутренней энергии для процесса возгонки 1 моль вещества в тройной точке; 27. определите число термодинамических степеней свободы при следующих значениях температуры и давления: нормальная температура кипения). Необходимые для расчета данные возьмите из таблицы. Вариант Твердое состояние Жидкое состояние Условия
Решение:
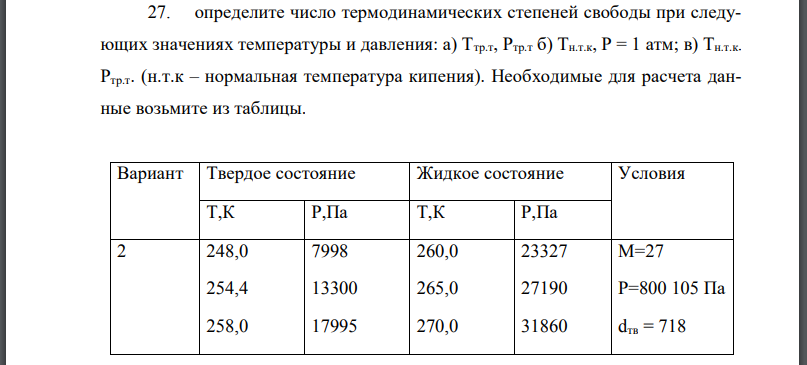
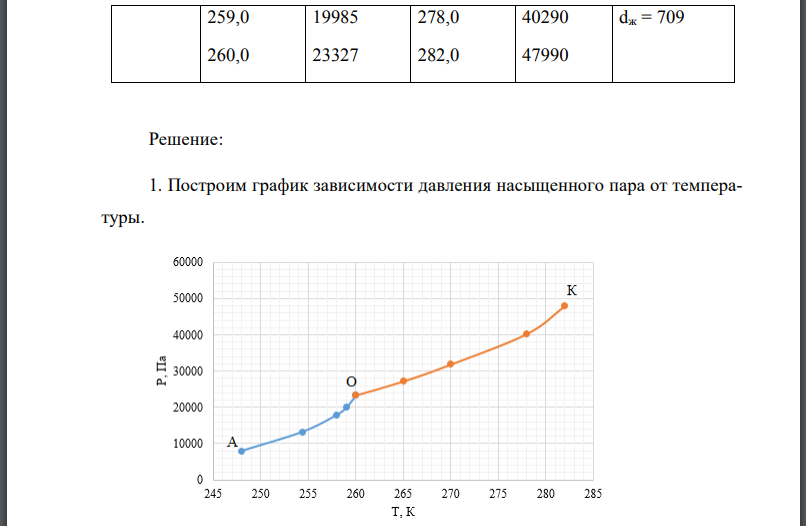
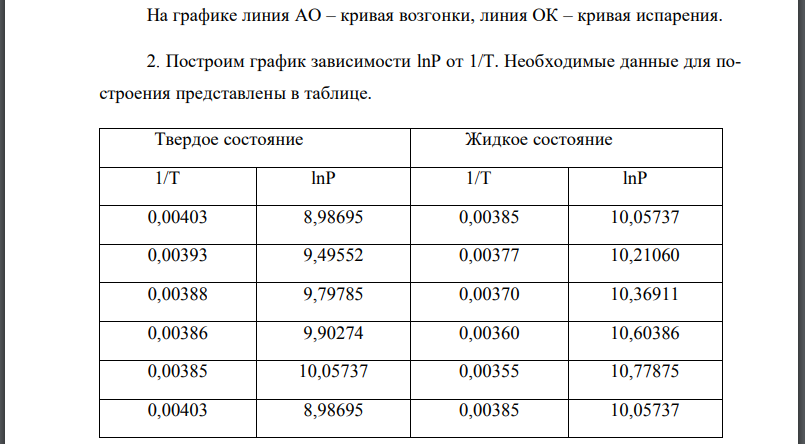
1. Построим график зависимости давления насыщенного пара от температуры. На графике линия кривая возгонки, линия кривая испарения. 2. Построим график зависимости Необходимые данные для построения представлены в таблице. Твердое состояние Жидкое состояние 3. Тройная точка лежит на пересечении прямых графика зависимости Координаты тройной точки: 4. Теплоты возгонки и испарения можно вычислить по тангенсам наклона прямых.Тангенсы угла наклона можно найти через отношения отрезков: Средняя теплота возгонки равна 5. Теплоту плавления можно вычислить по закону Гесса, если известны теплоты возгонки и испарения: 6. Величину для процесса плавления при температуре тройной точки определим с помощью уравнения Клапейрона-Клаузиса: температура плавления в тройной точке, Получаем Вычислим температуру плавления при 8. Изменение энтропии возгонки 1 моль вещества равно Изменение энергии Гиббса равно Изменение внутренней энергии равно Изменение энергии Гельмгольца: Число степеней свободы определим по правилу фаз Гиббса: В тройной точке число фаз Ф равно 3, число компонентов К равно Число фаз Ф равно 2, число компонентов К равно 1. Число фаз Ф равно 1, число компонентов К равно 
- навеску раствора пероксида водорода 10,00 г разбавили водой в мерной колбе на 100,0 мл. на титрование 10,00 мл этого раствора
- Из раствора сульфата железа (3) осадили железо раствором аммиака в виде гидроксида. Полученный осадок прокалили. Масса прокаленного
- Несовершенный поляризатор пропускает в своей плоскости 𝜂1= 0,9 часть интенсивности соответствующего колебания (т.е. колебаний, происходящих в плоскости пропускания поляризатора)
- При температуре Т давление пара раствора концентрации с неизвестного нелетучего вещества в жидком растворителе равно Р Па; плотность этого раствора d. Зависимость

