
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Навеску промедола гидрохлорида массой 0,5030 г перенесли в колбу для титрования, добавили HNO3, железоаммонийные квасцы
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16962 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
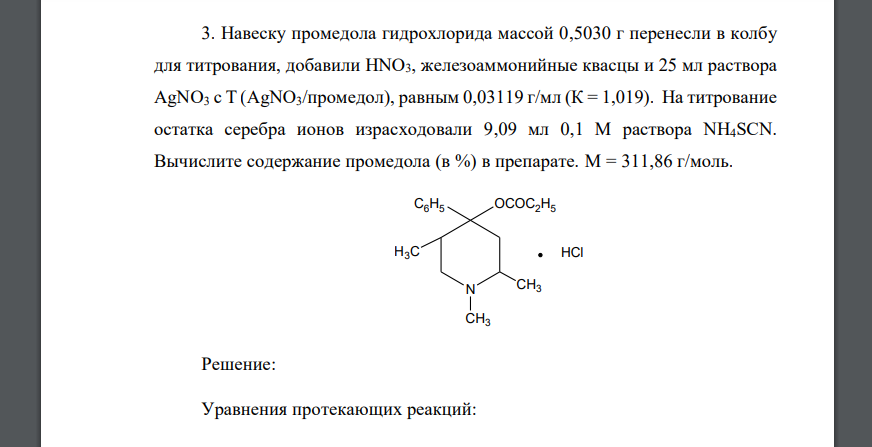
Навеску промедола гидрохлорида массой 0,5030 г перенесли в колбу для титрования, добавили HNO3, железоаммонийные квасцы и 25 мл раствора AgNO3 с Т (AgNO3/промедол), равным 0,03119 г/мл (К = 1,019). На титрование остатка серебра ионов израсходовали 9,09 мл 0,1 М раствора NH4SCN. Вычислите содержание промедола (в %) в препарате. М = 311,86 г/моль. N CH3 H3C C6H5 OCOC2H5 CH3 HCl
Решение:
Уравнения протекающих реакций: Рассчитаем массу промедола гидрохлорида в навеске
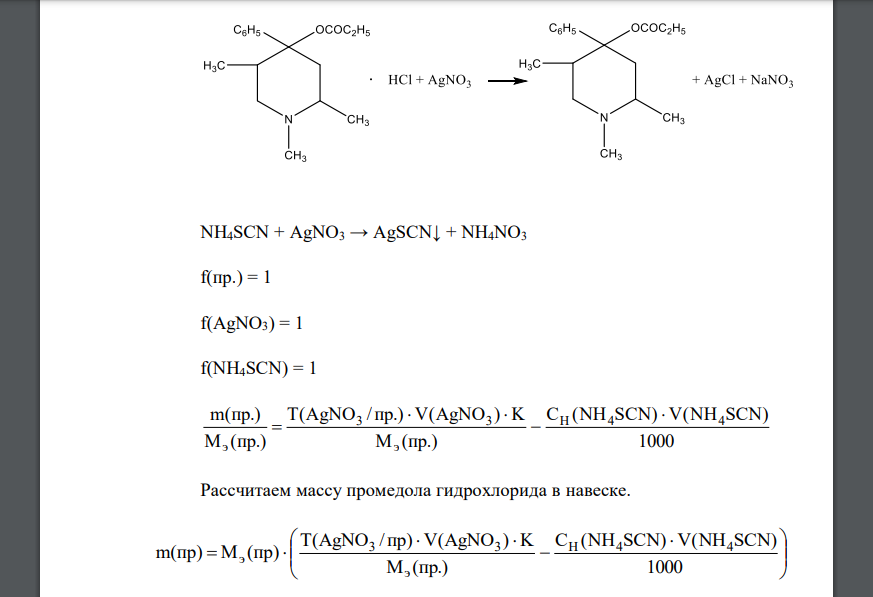
- Определите молярную концентрацию эквивалента и титр NaOH в растворе, если на титрование 5 мл этого раствора
- Сравните, как пойдет коррозия металлических сооружений: а) в воде - при низких и высоких температурах (зима - лето, север - юг); б) в водной и неводной частях
- К 98,1 мл раствора с концентрацией 10,2 моль/л и плотностью 1,163 г/см3 прибавили необходимое для нейтрализации количество раствора с массовой
- Какой объем 24%-ного раствора хлороводородной кислоты HCl (ρ = 1,12 г/мл) потребуется для приготовления 200 мл раствора

