
Нитрогенсодержащие органические соединения в химии с примерами
Содержание:
Нитрогенсодержащие органические соединения:
Органические соединения, в молекулах которых есть атомы Нитрогена, очень важны. Особое место среди них занимают белки. Благодаря этим соединениям существует жизнь на нашей планете. В синтезе белков, который происходит в живых организмах, участвуют нуклеиновые кислоты. Они сохраняют и воспроизводят генетическую информацию. Нитрогенсодержащими соединениями являются также многие физиологически активные вещества, стимулирующие или угнетающие различные биологические процессы в организме. Среди них — витамины, антибиотики, наркотики.
Ознакомление с нитрогенсодержащими органическими соединениями обычно начинают с аминов.
Метиламин
Амины: К классу аминов относятся многие соединения, образованные тремя элементами — Карбоном, Гидрогеном и Нитрогеном.
Амины — зто продукты замещении атомов Гидрогена в молекуле аммиака на углеводородные остатки.
Приводим схему замещения атома Гидрогена в молекуле аммиака на метильную группу 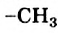
Амины различного состава и строения встречаются в природе. Эти соединения используют для производства полимеров, синтетических волокон, красителей, некоторых лекарственных препаратов.
Метиламин: Простейшим соединением класса аминов является метиламин 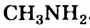 .
.
Строение молекулы. Молекула метиламина состоит из двух частей — углеводородного остатка 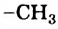 и аминогруппы
и аминогруппы 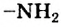 .
.
Атом Нитрогена в молекуле метиламина (рис. 108) образует три простых ковалентных связи — с атомом Карбона и двумя атомами Гидрогена.
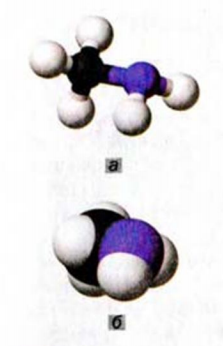
Рис. 108. Модели молекулы метиламина: а — шаро-стержневая; б — масштабная. Белые шарики — атомы Гидрогена, черные — атомы Карбона, синие — атомы Нитрогена
В этих связях участвуют три неспаренных электрона второго энергетического уровня атома Нитрогена:
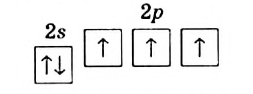
Кроме них, на этом уровне имеется пара 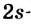 электронов.
электронов.
Поскольку Нитроген более электроотрицателен, чем Карбон и Гидроген, ковалентные связи атома этого элемента с другими атомами в молекуле метиламина наиболее полярны (рис. 109). Полярной является и сама молекула 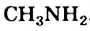 .
.
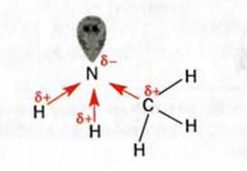
Рис. 109. Смещение общих электронных пар в молекуле метиламина
Физические свойства: В обычных условиях метиламин — газ с резким неприятным запахом. Соединение хорошо растворяется в воде (как вы думаете, почему?), спирте, ацетоне. Температура кипения метиламина -6,3 °С. Она намного выше, чем у соответствующего углеводорода — метана 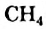 (-161,5°С). Это объясняется существованием между молекулами метиламина водородных связей.
(-161,5°С). Это объясняется существованием между молекулами метиламина водородных связей.
Химические свойства: Способность метиламина вступать в реакции, рассмотренные ниже, обусловлена наличием в атоме Нитрогена «неподеленной» пары 28-электронов.
Реакция с водой: Метиламин в водном растворе проявляет основные свойства. Количество ионов 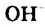 в нем значительно больше, чем в чистой воде. Что же происходит в этом растворе? Между молекулами воды и метиламина образуются водородные связи
в нем значительно больше, чем в чистой воде. Что же происходит в этом растворе? Между молекулами воды и метиламина образуются водородные связи
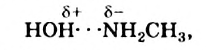
которые вызывают диссоциацию многих молекул воды:
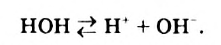
Ионы 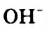 остаются в растворе, обуславливая его щелочную реакцию, а ионы
остаются в растворе, обуславливая его щелочную реакцию, а ионы 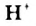 соединяются с молекулами метиламина
соединяются с молекулами метиламина 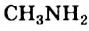 .
.
Объясним, почему происходит такое соединение. В ионе 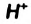 нет электронов;
нет электронов; 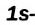 -орбиталь в нем вакантная. При контакте частиц
-орбиталь в нем вакантная. При контакте частиц 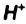 и
и 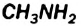 в эту орбиталь переходит пара
в эту орбиталь переходит пара 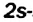 электронов атома Нитрогена, и частицы соединяются:
электронов атома Нитрогена, и частицы соединяются:
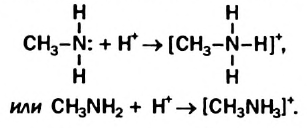
Таким образом, атом Нитрогена образует четвертую связь. Поскольку эту связь обеспечивает пара электронов, то она является кова-лентной, как и три другие связи атома Нитрогена.
Суммарная схема взаимодействия метиламина с водой:
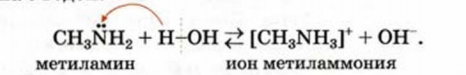
Щелочную среду в водном растворе метиламина можно обнаружить с помощью индикатора.
Если основания 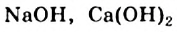 и др. мы характеризовали как соединения, диссоциирующие с образованием ионов
и др. мы характеризовали как соединения, диссоциирующие с образованием ионов 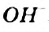 , то метиламин
, то метиламин 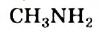 — тоже основание, но иного типа. Его основные свойства обусловлены способностью молекул присоединять катионы
— тоже основание, но иного типа. Его основные свойства обусловлены способностью молекул присоединять катионы 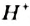 .
.
Это интересно: Соединяться с ионом 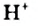 может и молекула аммиака:
может и молекула аммиака: 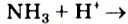
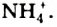
Реакции с кислотами: Метиламин взаимодействует с кислотами. Продуктами таких реакций являются соли — ионные соединения, растворимые в воде:
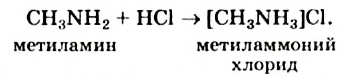
Преобразуем молекулярное уравнение в ионно-молекулярное:
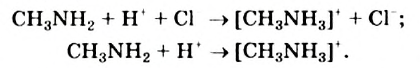
Реакция горения: Метиламин горит на воздухе:
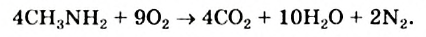
Смеси метиламина с воздухом взрывоопасны.
Применение: Метиламин используют для производства лекарств, красителей, растворителей, средств защиты растений от болезней и вредителей.
Физиологическое действие: Метиламин — токсичное соединение. Он раздражает слизистые оболочки, угнетает дыхание, отрицательно действует на нервную систему, внутренние органы.
Выводы:
- Амины — продукты замещения атомов Гидрогена в молекуле аммиака
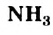 на углеводородные остатки.
на углеводородные остатки. - Простейшим по составу амином является метиламин
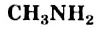 . Молекула соединения содержит группу атомов
. Молекула соединения содержит группу атомов 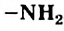 ; ее называют аминогруппой.
; ее называют аминогруппой. - Метиламин — токсичный газ с резким запахом, хорошо растворимый в воде. Водный раствор этого соединения содержит ионы
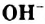 . Метиламин — органическое основание. Он взаимодействует с кислотами, образуя соли, содержащие катионы
. Метиламин — органическое основание. Он взаимодействует с кислотами, образуя соли, содержащие катионы 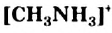 .
.
Аминокислоты. Аминоуксусная кислота
Аминокислоты: Существуют органические соединения, которые играют очень важную роль в природе. Это аминокислоты.
Аминокислоты — производные углеводородов, в молекулах которых имеются аминогруппы и карбоксильные группы.
Пример замещения атомов Гидрогена в молекуле углеводорода на соответствующие функциональные группы:
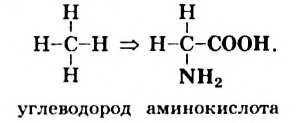
Кислоты, в молекулах которых аминогруппа соединена с атомом Карбона, ближайшим к карбоксильной группе, называют 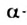 аминокислотами.
аминокислотами.
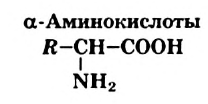
Двадцать строго определенных аминокислот составляют основу белков. Часть этих аминокислот образуется в клетках из продуктов обмена веществ; их называют заменимыми. Другие, незаменимые 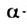 аминокислоты, человек и животные получают вместе с пищей. Некоторые
аминокислоты, человек и животные получают вместе с пищей. Некоторые 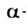 аминокислоты являются антибиотиками, витаминами.
аминокислоты являются антибиотиками, витаминами.
Для 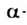 аминокислот чаще используют тривиальные названия. Кроме того, эти соединения обозначают символами. Каждый символ состоит из трех первых букв тривиального названия аминокислоты.
аминокислот чаще используют тривиальные названия. Кроме того, эти соединения обозначают символами. Каждый символ состоит из трех первых букв тривиального названия аминокислоты.
Аминоуксусная кислота: Простейшей 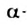 аминокислотой является аминоуксусная кислота
аминокислотой является аминоуксусная кислота 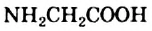 (рис. 110). Ее тривиальное название — глицин. Название происходит от греческого слова glykys - сладкий. Сокращенные обозначения (символы) соединения — Гли, Gly.
(рис. 110). Ее тривиальное название — глицин. Название происходит от греческого слова glykys - сладкий. Сокращенные обозначения (символы) соединения — Гли, Gly.
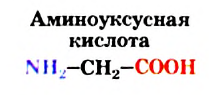
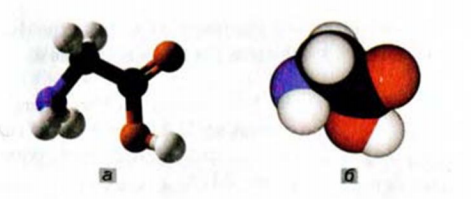
Рис. 110. Модели молекулы аминоуксусной кислоты: а — шаро-стержневая; б — масштабная
Физические свойства: Аминоуксусная кислота (глицин) — кристаллическое вещество (рис. 111), имеющее сладкий вкус, растворимое в воде и нерастворимое в органических растворителях.
Рис. 111. Аминоуксусная кислота (глицин)
Химические свойства: В молекуле аминоуксусной кислоты имеются две функциональные группы: карбоксильная 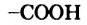 и аминогруппа
и аминогруппа 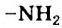 . Первая обуславливает кислотные свойства соединения, а вторая — основные. Поэтому аминоуксусная кислота является амфотерным соединением. Она реагирует и со щелочами, и с кислотами. Продуктами таких реакций являются соли.
. Первая обуславливает кислотные свойства соединения, а вторая — основные. Поэтому аминоуксусная кислота является амфотерным соединением. Она реагирует и со щелочами, и с кислотами. Продуктами таких реакций являются соли.
Во взаимодействии аминоуксусной кислоты (глицина) со щелочью принимают участие карбоксильные группы ее молекул
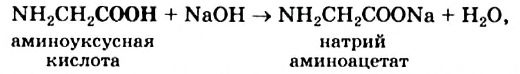
а в реакции с сильной кислотой — аминогруппы:
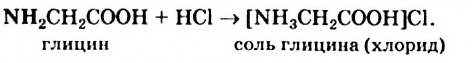
Аминоуксусная кислота (в растворе), как и карбоновые кислоты, вступает в реакции с активными металлами, основными оксидами, основаниями, некоторыми солями, спиртами.
Аминоуксусная кислота взаимодействует с купрум(II) гидроксидом (в щелочной среде); при этом образуется раствор синего цвета (рис. 112).
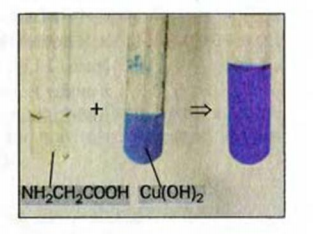
Рис. 112. Реакция раствора аминоуксусной кислоты с купрум(II) гидроксидом
Реакции между аминокислотами: В определенных условиях молекулы аминоуксусной и других 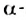 аминокислот могут взаимодействовать друг с другом. Продуктами таких реакций являются пептиды. Термин происходит от греческого слова peptos — сваренный.
аминокислот могут взаимодействовать друг с другом. Продуктами таких реакций являются пептиды. Термин происходит от греческого слова peptos — сваренный.
Приводим схему образования дипептида из двух молекул аминоуксусной кислоты:
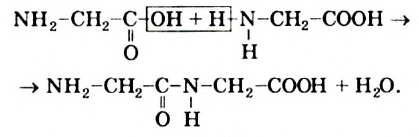
Эта реакция обратима. Противоположное превращение — гидролиз дипептида — происходит при нагревании в присутствии сильных кислот или щелочей.
В молекуле дипептида, как и аминокислоты, имеются аминогруппа и карбоксильная группа. Любая из этих групп может реагировать с соответствующей группой другой молекулы аминокислоты с образованием молекулы трипептида. Из многих молекул аминокислот образуются полипептиды.
Молекулы пептидов содержат одинаковые группы атомов, которые называют пептидными группами:
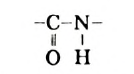
Образование полипептидов из 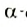 аминокислот составляет основу синтеза белков в живом организме.
аминокислот составляет основу синтеза белков в живом организме.
Применение: Аминокислоты широко используют как лекарственные препараты при заболеваниях крови, печени, поджелудочной железы, нарушениях нервной системы и обмена веществ. Некоторые аминокислоты обезвреживают токсичные вещества в организме, являются пищевыми добавками для животных, сырьем для производства синтетических волокон, пластмасс.
Аминоуксусную кислоту (глицин) используют как исходное вещество для получения органических соединений, в медицине, иногда — для обработки кинофотоматериалов.
Это интересно: Вкус натриевой соли глутаминовой кислоты напоминает вкус мяса. Это соединение используют в качестве приправы.
Выводы:
- Аминокислоты — производные углеводородов, в молекулах которых имеются аминогруппы и карбоксильные группы. Если аминогруппа соединена с атомом Карбона, ближайшим к карбоксильной группе, то такие соединения называют
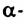 аминокислотами.
аминокислотами. - Фрагменты молекул двадцати
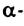 аминокислот входят в состав молекул белков.
аминокислот входят в состав молекул белков. - Простейшая
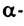 аминокислота — аминоуксусная
аминокислота — аминоуксусная 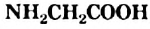 . Это кристаллическое вещество со сладким вкусом. Аминоуксусная кислота является амфотериым соединением; она реагирует со щелочами и сильными кислотами.
. Это кристаллическое вещество со сладким вкусом. Аминоуксусная кислота является амфотериым соединением; она реагирует со щелочами и сильными кислотами. - Молекулы аминоуксусной и других аминокислот могут взаимодействовать друг с другом. При этом образуются пептиды — соединения, молекулы которых содержат остатки молекул аминокислот, соединенные группами атомов
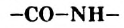 (пептидными группами).
(пептидными группами). - Аминокислоты используют в медицине, производстве полимерных материалов, добавляют в корма сельскохозяйственных животных.
Белки
В природе нашей планеты есть вещества, без которых существование живых организмов было бы невозможным. Это — белки.
Белки — полипеитиды, выполняющие специфические биологические функции в живых орг анизмах.
Известно очень много белков. Они осуществляют и регулируют обмен веществ в клетках, в то же время являясь для них «строительным» материалом. Белки реагируют на изменение внешней среды, изменяясь и приспосабливаясь к новым условиям. Они обеспечивают двигательную деятельность организма, а некоторые (так называемые белки-антитела) защищают его от инородных тел. Все реакции в клетках происходят при участии белков-ферментов, которые играют роль катализаторов. Таким образом, белки выполняют в организме разнообразные функции — энергетическую, строительную, сигнальную, двигательную, защитную, каталитическую.
Каждый белок отличается от других набором аминокислотных остатков, их строго определенной последовательностью в молекуле, пространственным строением молекул, а также осуществляемыми функциями.
В организмах животных и человека содержится больше белков, чем в растениях. Они входят в состав мышечной и нервной тканей, кожи, волос, ногтей.
Вырабатывать белки непосредственно из неорганических веществ могут только растения. В них и некоторых бактериях белки образуются в результате фотосинтеза (как и углеводы):

В организмы животных и человека белки поступают с пищей. Они расщепляются ферментами на аминокислоты, из которых образуются другие белки, свойственные данному организму.
Во всех белках содержатся пять основных элементов — Карбон (его массовая доля составляет 50—55 %), Оксиген (21,5—23,5 %), Нитроген (15—17 %), Гидроген (6,5—7,3 %), Сульфур (0,3—2,5 %), а также небольшие количества Фосфора, Иода, Феррума, других элементов.
Белки имеют высокие значения молекулярных масс — от десятков тысяч до нескольких миллионов. Химические формулы этих соединений очень сложные.
Это интересно: При полном расщеплении белка выделяется свыше 17 кДж энергии.
Классификация: Различают простые и сложные белки. Молекулы простых белков1 состоят только из остатков молекул аминокислот, а сложных2 содержат также остатки молекул соединений небелковой природы (углеводов, ортофосфатной кислоты 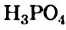 , нуклеиновых кислот и др.).
, нуклеиновых кислот и др.).
Простые белки называют протеинами (от греческого слова 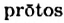 — первый), а сложные - протеидами (от греческих слов
— первый), а сложные - протеидами (от греческих слов 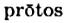 — первый и eidos — вид).
— первый и eidos — вид).
Строение молекул: Уникальность белков обусловлена их строением, которого не имеет ни одно из изученных вами соединений. Первый весомый вклад в исследование белков внес немецкий ученый Э. Фишер. Он доказал, что их молекулы построены из остатков молекул 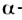 аминокислот, соединенных пептидными группами. Различают четыре типа структуры белка.
аминокислот, соединенных пептидными группами. Различают четыре типа структуры белка.
Первичная структура белка — это полипептидная цепь со строго определенной последовательностью аминокислотных остатков (рис. 113):
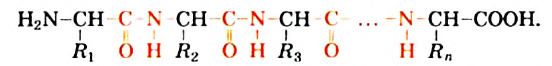
В приведенной формуле буквами 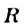 с различными индексами обозначены углеводородные и другие остатки.
с различными индексами обозначены углеводородные и другие остатки.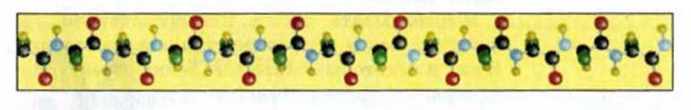
Рис. 113. Шаростержневая модель фрагмента первичной структуры белка. Черные шарики — атомы Карбона, желтые — Гидрогена, голубые — Нитрогена, красные — Оксигена. Зеленые шарики имитируют углеводородные остатки
Эмиль Герман Фишер (1852-1919)

Немецкий химик и биохимик, академик Берлинской академии наук. Исследовал белки и продукты их расщепления. Доказал, что при взаимодействии аминокислот образуются полипептиды. Изучал действие ферментов на различные соединения. Разработал классификацию углеводов и методы их синтеза. Внес значительный вклад в развитие стереохимии. Лауреат Нобелевской премии (1902).
Вторичная структура белка — это определенная пространственная форма (большей частью — спираль), которую приобретает полипептидная цепь (рис. 114).
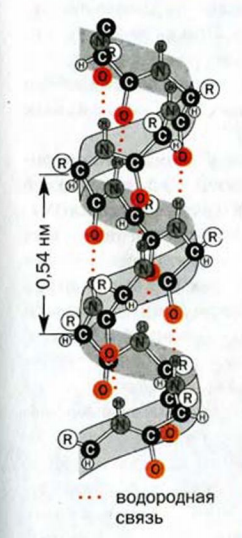
Рис. 114. Вторичная структура белка
Третичная структура белка образуется в результате свертывания спирали полипептидной цепи в более компактную форму (глобулу) (рис. 115).
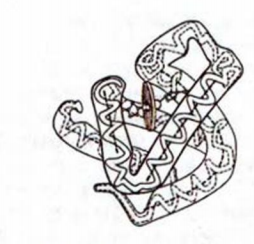
Рис. 115. Третичная структура белка
Четвертичная структура белка является системой очень сложной формы. В ней объединены две или больше глобул. Образуется единый комплекс, который выполняет определенную функцию в живом организме.
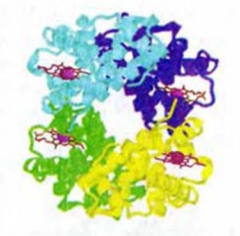
Рис. 116. Четвертичная структура белка (молекула гемоглобина)
Четвертичную структуру имеют лишь некоторые белки, например, гемоглобин; его молекула содержит четыре глобулы (рис. 116).
- Учитывая форму молекул, белки делят на фибриллярные и глобулярные. Фибриллярные белки имеют нитевидные молекулы, не растворяются в воде. Из них состоят волокна живых тканей, шелк, шерсть, волосы, рога, когти. Глобулярные белки отличаются от фибриллярных компактной формой молекул и достаточной растворимостью в воде. Они регулируют биохимические процессы. К этой группе белков относятся ферменты, многие гормоны, гемоглобин и др.
Физические свойства: Белки не имеют температур плавления и кипения. При нагревании они темнеют и начинают разлагаться, распространяя запах жженых перьев. Некоторые белки растворяются в воде с образованием коллоидных растворов.
При добавлении к раствору белка концентрированных растворов кислот, щелочей, солей Купрума(II), Плюмбума(II), других («тяжелых») металлических элементов, а также органических растворителей (например, спирта) происходит осаждение белка (денатурация - термин происходит от греческого слова denaturatus — лишенный природных свойств). Аналогичный эффект наблюдается при нагревании. Он вызван разрушением четвертичной, третичной и вторичной структур белка. В результате белок теряет способность выполнять свои биологические функции. Но пищевые продукты после денатурации белков легче усваиваются организмом — яичница или сваренное яйцо по сравнению с сырым, кислое молоко по сравнению со свежим.
Химические свойства: Белки, как и аминокислоты, являются амфотерными соединения ми со слабо выраженными основными и кислотными свойствами.
В присутствии кислот или ферментов белки подвергаются гидролизу. Конечными продуктами этого превращения являются аминокислоты, из которых образовался белок. Гидролиз происходит в несколько стадий:
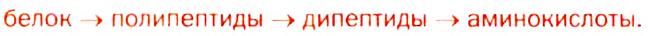
Некоторые реакции с участием белков сопровождаются изменением цвета, поэтому их называют цветными. К ним относятся биуретовая (Название происходит от аналогичной реакции, в которую вступает нитрогенсодержащее соединение — биурет.), ксантопротеиновая (Название происходит от греческих слов xanthos — желтый и prfltos — первый) реакции и др.
Практическое значение: Белки являются важнейшей составляющей нашего питания и рациона животных. Их ценность определяется наличием в молекулах белков фрагментов молекул незаменимых аминокислот. Недостаток белков в пище отрицательно влияет на организм, вызывает некоторые заболевания. В животноводстве и птицеводстве с целью увеличения пищевой ценности кормов их обогащают искусственными белками, произведенными с помощью микробиологического синтеза.
Это интересно: Суточная потребность в белках взрослого человека составляет в среднем 100-110 г.
Вещества и материалы, основу которых составляют белки, имеют широкое применение. Среди них — шерсть, шелк, кожа, меха, клен, желатин и др. В современные стиральные порошки вводят биодобавки — ферменты, катализирующие распад белковых загрязнений белья и одежды. Белки используют и в медицине.
Синтез белков: В живых организмах синтез белков происходит при участии нуклеиновых кислот. Эти соединения рассмотрим в следующем параграфе.
Выводы:
- Белки — полипептиды, «построенные» из остатков молекул
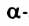 аминокислот и выполняющие специфические биологические функции в живых организмах. Эти соединения осуществляют и регулируют обмен веществ в клетках, а также являются для них «строительным» мате риалом. В организмы животных и человека белки поступают с пищей. Они расщепляются ферментами на аминокислоты, из которых обра зуютсн другие белки, свойственные данному организму.
аминокислот и выполняющие специфические биологические функции в живых организмах. Эти соединения осуществляют и регулируют обмен веществ в клетках, а также являются для них «строительным» мате риалом. В организмы животных и человека белки поступают с пищей. Они расщепляются ферментами на аминокислоты, из которых обра зуютсн другие белки, свойственные данному организму. - В белках содержатся Карбон, Океиген, Нитро-ген, Гидроген, Сульфур, а иногда и некоторые другие элементы.
- Различают первичную, вторичную, третичную и четвертичную структуры белка.
- При нагревании раствора белка или добавлении к нему кислот, щелочей, некоторых солей происходит его денатурация, т. е. разрушение пространственной структуры и потеря биологических функций. В присутствии кислот, щелочей или ферментов белки подвергаются гидролизу.
Нуклеиновые кислоты
Способность организмов передавать следующим поколениям свои признаки, а также тип обмена веществ называют наследственностью. Ученые обнаружили, что за наследственность «отвечают» соединения очень сложного строения — нуклеиновые кислоты. Термин происходит от латинского слова nucleus — ядро (нуклеиновые кислоты были впервые обнаружены в ядрах клеток).
Нуклеиновые кислоты — зто высокомолекулярные (соединения, молекулы которых состоят из чрезвычайно большого числа атомов; к ним принадлежат, в частности, крахмал, целлюлоза, полиэтилен) природные соединения, которые сохраняют и воспроизводят в организмах генетическую информацию, а также принимают участие в синтезе белков.
Существуют два вида нуклеиновых кислот: рибонуклеиновые (сокращенное обозначение — РНК) и дезоксирибонуклеиновые (ДНК). Их названия происходят от названий моносахаридов — рибозы 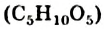 и дезоксирибозы
и дезоксирибозы 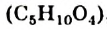 , остатки молекул которых содержатся в молекулах нуклеиновых кислот. В клетках живых организмов количество молекул РНК превышает количество молекул ДНК.
, остатки молекул которых содержатся в молекулах нуклеиновых кислот. В клетках живых организмов количество молекул РНК превышает количество молекул ДНК.
Значения относительных молекулярных масс ДНК составляют несколько десятков миллионов, а РНК — от 20 тысяч до нескольких миллионов.
Строение молекул: Нуклеиновые кислоты, как и белки, являются природными полимерами. Если молекула белка состоит из остатков молекул аминокислот, то молекула нуклеиновой кислоты — из остатков молекул ортофосфатной кислоты 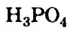 , моносахарида и некоторых нитрогенсодержащих соединений. Три соединенных остатка различного типа называют нуклеотидом.
, моносахарида и некоторых нитрогенсодержащих соединений. Три соединенных остатка различного типа называют нуклеотидом.
Упрощенно нуклеотид можно изобразить так:
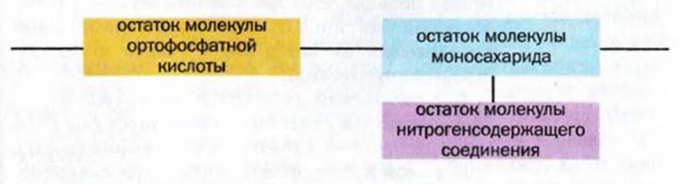
Цепь молекулы нуклеиновой кислоты получила название полинуклеотидной (молекулы белков имеют полипептидную цепь). Приводим схему ее строения:
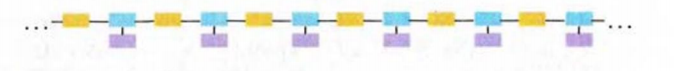
Пространственное строение молекул нуклеиновых кислот напоминает строение молекул белков. Молекула ДНК имеет первичную, вторичную и третичную структуры, а РНК — только первичную, но определенные ее участки вследствие образования водородных связей «закручиваются», формируя вторичную или даже третичную структуры.
Молекула ДНК состоит из двух полинуклеотидных цепей (рис. 118), закрученных вокруг общей оси. Остатки молекул нитрогенсодержащих соединений расположены внутри спирали и перпендикулярно ее оси, а остатки молекул ортофосфатной кислоты и моносахарида образуют каркас молекулы ДНК. Обе цепи молекулы ДНК удерживаются вместе с помощью водородных связей, существующих между различными остатками молекул нитрогенсодержащих соединений.
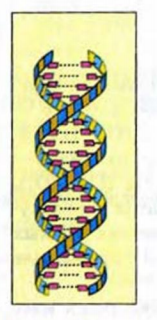
Рис. 118. Упрощенная модель молекулы ДНК
Функции нуклеиновых кислот: Биологическая роль ДНК в организме состоит в сохранении генетической информации. Такая информация, присущая данному биологическому виду, «записана» в молекуле ДНК строго определенной последовательностью нуклеотидов. Эта информация используется для синтеза белков и рибонуклеиновых кислот. Единицей генетической информации является ген — часть молекулы ДНК (тринуклеотид).
Биологическая роль РНК в организме — осуществление синтеза белков (молекулы ДНК непосредственного участия в нем не принимают).
В живой клетке есть три вида рибонуклеиновых кислот: информационные, транспортные и рибосомные. Информационная РНК «копирует» определенный участок молекулы ДНК и служит основой (матрицей) для биосинтеза белка. Последовательность нуклеотидов на этом участке отвечает последовательности аминокислотных остатков в молекуле белка. (Именно поэтому ДНК отвечает за структуру белков определенного организма.) Эту последовательность (код) расшифровывает транспортная РНК и «переносит» молекулы аминокислот к месту синтеза белка. Каждой аминокислоте соответствует своя транспортная РНК. Рибосомная РНК принимает участие в биосинтезе белка.
Воспроизведение каждой ДНК и ее передача от предыдущего поколения последующему обеспечивают синтез одних и тех же белков. Этим объясняется сохранение специфических признаков данного вида организмов.
Свойства: ДНК и РНК растворяются в воде с образованием коллоидных растворов, при нагревании которых они осаждаются, теряя свои биологические функции.
Радиоактивное излучение, а также некоторые вещества вызывают изменения в последовательности расположения нуклеотидов в молекуле ДНК. Это может привести к ошибкам в передаче генетической информации, синтезе белка и, как следствие, к заболеванию организма или даже его гибели.
Генная инженерия: Исследования нуклеиновых кислот положили начало новому направлению биологической науки — генной инженерии. Появилась возможность руководить процессами, происходящими в живой клетке, синтезировать в ней «запрограммированные» белки. Открылись широкие перспективы в решении таких глобальных проблем, как нехватка продуктов питания, борьба с неизлечимыми болезнями. Ученые уже вывели генетически модифицированные сорта картофеля, кукурузы, сои, сахарной свеклы, других сельскохозяйственных культур. Новые растения оказались устойчивыми к болезням и вредителям. Они дружно созревают, дают высокие урожаи, хорошо хранятся и транспортируются.
Это интересно. Применение трансгенной технологии в животноводстве позволяет увеличить содержание белков в молоке.
Возможно, вскоре будут выведены растения и животные, которых в природе не существует.
Использование достижений генной инженерии должно быть под строгим контролем. Пищевые продукты с «инородными» для человека белками могут оказаться токсичными, вызывать аллергию. Перед тем, как внедрять генетически модифицированные растения, необходимо проводить разносторонние и комплексные исследования, чтобы не причинить серьезного вреда существующим видам организмов. Ученые-генетики не должны переступать границу, за которой результаты их работы отрицательно повлияют на здоровье людей и окружающую среду.
Выводы:
- Нуклеиновые кислоты — высокомолекулярные природные соединения, которые сохраняют н воспроизводят в организмах генетическую информацию, а также принимают участие в синтезе белков.
- Молекула нуклеиновой кислоты состоит из огромного числа нуклеотидов, в каждом из которых содержатся остатки молекул ортофосфатной кислоты, моносахарида и нитрогенсодержащего соединения.
- Существуют рибонуклеиновые (РНК) и дезоксирибонуклеиновые (ДНК) кислоты. Биологическая роль ДНК в организме состоит в сохранении и передаче последующему поколению генетической информации, а РНК — в осуществлении синтеза белков.
- Ученые, работающие в области генной инженерии, разрабатывают методы конструирования молекул ДНК. Это открывает широкие перспективы в решении проблем сельского хозяйства, здравоохранения. Вместе с тем необходимо выяснить, не причинят ли вреда человеку пищевые продукты, содержащие генномодифицированные компоненты.
Физиологически активные вещества
Существует большая группа органических соединений, которые ввиду их особого воздействия на организм назвали физиологически активными веществами.
Физиологически активные вещества — это органические соединения, активно влияющие на различные биологические процессы в живых организмах.
Такие вещества были вначале обнаружены в грибах, растениях, животных, а со временем их научились синтезировать в лаборатории.
220
К физиологически активным веществам относят витамины, алкалоиды, антибиотики, гормоны и др.
Антибиотиками называют органические вещества, обладающие способностью препятствовать росту и размножению микробов, бактерий. В природе их вырабатывают некоторые микроорганизмы (например, плесень), растения и животные. Гормоны регулируют протекание химических процессов в организме.
В этом параграфе рассмотрим витамины и алкалоиды.
Витамины: Человеку для обеспечения нормальной жизнедеятельности кроме воды, белков, жиров, углеводов, солей необходимы витамины. Термин происходит от латинского слова vita — жизнь и названия класса соединений — амины (часть витаминов является их производными). Их главным источником являются растения (рис. 119), однако некоторые витамины образуются в организмах животных и человека.
Витамины — органические соединении, которые необходимы организму и незначительных количествах дли осуществлении важных биохимических процессов.

Рис. 119. Некоторые природные источники витаминов
Известно около 20 витаминов. Они имеют сложные формулы и химические названия. Для удобства эти соединения обозначают большими латинскими буквами (А, В, С и др.), иногда с числовыми индексами (например, 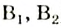 ). Одну и ту же букву используют для обозначения витаминов, выполняющих в организме подобные функции.
). Одну и ту же букву используют для обозначения витаминов, выполняющих в организме подобные функции.
Витамины делят на водорастворимые и жирорастворимые.
Водорастворимые витамины. В воде растворяются витамин С, витамины группы В 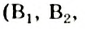
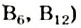 и некоторые другие.Витамин С (аскорбиновая кислота) является одним из важнейших. Он участвует в образовании белков и желчных кислот, усиливает сопротивляемость организма различным инфекциям, улучшает состояние кожи, ускоряет ее заживление. При недостатке этого витамина в пищевых продуктах человек заболевает цингой, у него начинают кровоточить десны, ослабевает скелет, происходят изменения в нервной и кровеносной системах.
и некоторые другие.Витамин С (аскорбиновая кислота) является одним из важнейших. Он участвует в образовании белков и желчных кислот, усиливает сопротивляемость организма различным инфекциям, улучшает состояние кожи, ускоряет ее заживление. При недостатке этого витамина в пищевых продуктах человек заболевает цингой, у него начинают кровоточить десны, ослабевает скелет, происходят изменения в нервной и кровеносной системах.
Это интересно: Витамин С добавляют в безалкогольные напитки, сладости, продукты для детского питания.
Формула витамина С — 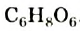 . Это белое кристаллическое вещество. Водный раствор витамина С проявляет кислотные свойства; соединение действует на индикаторы, реагирует со щелочами, некоторыми солями, а также вступает в окислительно-восстановительные реакции (рис. 120). Этот витамин в водном растворе, на свету или при нагревании разлагается.
. Это белое кристаллическое вещество. Водный раствор витамина С проявляет кислотные свойства; соединение действует на индикаторы, реагирует со щелочами, некоторыми солями, а также вступает в окислительно-восстановительные реакции (рис. 120). Этот витамин в водном растворе, на свету или при нагревании разлагается.

Рис. 120. Опыты с раствором витамина С: а — действие на универсальный индикатор; б — реакция с натрий карбонатом; в — реакция с раствором калий перманганата
Витамин С содержится в шиповнике, орехах, черной смородине, сладком перце, хрене, цитрусовых и др.
- Витамины группы В входят в состав ферментов и отвечают за их каталитическую активность. Витамин
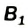 участвует в обмене веществ. Его недостаток в организме человека приводит к заболеванию нервной системы, нарушениям сердечной деятельности. Витамин
участвует в обмене веществ. Его недостаток в организме человека приводит к заболеванию нервной системы, нарушениям сердечной деятельности. Витамин 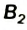 принимает участие в процессах окисления белков, жиров и углеводов. Он необходим при заболеваниях глаз, кожи.
принимает участие в процессах окисления белков, жиров и углеводов. Он необходим при заболеваниях глаз, кожи.
Витамины группы В содержатся в растительных и мясных продуктах, в частности, в зародышах пшеницы, дрожжах, молоке, яичном желтке, печени.
Жирорастворимые витамины: К витаминам этой группы относятся витамины A, D и некоторые другие.
Витамин А (ретинол) называют витамином роста. Он необходим для нормального развития организма, прежде всего молодого, увеличивает устойчивость к инфекционным заболеваниям. Его недостаток вызывает «куриную слепоту» — нарушение зрения при слабом освещении.
Витамин А — желтоватое вещество, которое разрушается в кислой среде и окисляется на воздухе (быстрее — на солнечном свету).
Витамин А содержится только в пищевых продуктах животного происхождения — рыбьем жире, печени (в частности, тресковой), яичном желтке, молоке.
Заменителем этого витамина является соединение, название которого — каротин. Его молекулы расщепляются в организме на две молекулы витамина А. Органические соединения, способные превращаться в витамины, называют провитаминами. Каротин — это провитамин А. Он содержится в моркови, тыкве, помидорах, некоторых фруктах, ягодах и обуславливает их оранжевый или красный цвет.
В организме человека и животных вырабатываются лишь некоторые витамины, причем в недостаточном количестве. Поэтому они должны поступать в организм вместе с пищевыми продуктами. Для укрепления здоровья, скорейшего выздоровления врачи рекомендуют принимать различные витаминные препараты.
Это интересно: В корма для сельскохозяйственных животных часто добавляют витамины 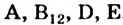 , поскольку их в растениях недостаточно.
, поскольку их в растениях недостаточно.
Суточная потребность человека в витаминах составляет от нескольких микрограммов до нескольких миллиграммов, а в витамине С — 50—60 мг. 1 микрограмм (1 мкг) равен 10 u грамма.
Жирорастворимых витаминов организму нужно значительно меньше, чем водора створимых.Существует группа лекарственных препаратов, название которой — поливитамины. Они содержат, помимо витаминов, также глюкозу, сахар, крахмал, пищевые красители. Хорошо известны отечественные поливитаминные препараты «Ревит», «Гексавит», «Декамевит» (рис. 121).

Рис. 121. Витаминные препараты
Существенный недостаток витаминов в пищевых продуктах или нарушение их усвояемости приводит к авитаминозу. Греческое а — приставка, означающая отрицание.
При употреблении витаминов в чрезмерном количестве, прежде всего А и D (в больших дозах они токсичны), возникает гипервитаминоз. Греческое 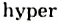 — приставка со значением «сверх».
— приставка со значением «сверх».
Алкалоиды: Люди еще в древности замечали, что при употреблении соков или отваров некоторых растений появляется бодрость, дополнительная энергия, проходит боль и усталость. Физиологически активные вещества, которые содержатся в этих соках и отварах, ученые назвали алкалоидами.
Алкалоиды — нитрогенсодержащие органические соединения, оказывающие сильное физиологическое действие на организмы животных н человека.
Известны несколько тысяч алкалоидов. Они содержатся в семенах и стеблях мака, бобах какао, плодах кофейного дерева, в листьях чая (рис. 122) и табака, коре хинного дерева, некоторых грибах и водорослях. Названия некоторых алкалоидов происходят от названий растений.

Рис. 122. Некоторые источники алкалоидов
Молекулы алкалоидов состоят из атомов Карбона, Гидрогена и Нитрогена, а иногда еще и Оксигена. Все эти соединения, как и амины, проявляют основные свойства (название «алкалоиды» означает «похожие на щелочи»); они реагируют с кислотами с образованием соответствующих солей.Алкалоиды кофеин (содержится в зернах кофе, чайных листьях) и теобромин (в бобах какао, шоколаде, чайных листьях) благотворно влияют на организм человека. После чашки кофе или крепкого чая исчезает усталость, повышается умственная и физическая активность.
Это интересно. Алкалоид хинин был первым эффективным противомалярийным средством. Он содержится в коре хинного дерева.
Алкалоид никотин (содержится в табаке1) — сильный яд; его смертельная доза — 40 мг. Он действует на нервную и кровеносную системы. В действительности растение содержит соли никотина, образованные им как органическим основанием, и кислотами — уксусной, лимонной,яблочной.
Никотин вызывает вредную привычку — курение.
О вреде курения: О том, что курить вредно, знают все. Тем не менее курильщики составляют значительную часть человечества. Известно, что в табачном дыме содержатся чрезвычайно вредные вещества, в частности, никотин, а также карбон(II) оксид (угарный газ). Попадая в легкие, этот газ блокирует способность гемоглобина переносить кислород к клеткам организма. Кроме этого, при горении сигареты происходят различные реакции и образуются свыше 3600 соединений, в том числе очень вредных. Дым сигареты содержит и вещества-канцерогены (они вызывают появление злокачественных опухолей). Смола от табачного дыма накапливается в легких. По статистике, курильщики болеют раком легких в 10 раз чаще, чем люди, не имеющие этой вредной привычки.
Табачный дым вредит не только курильщикам, но и тем, кто находится рядом и вынужден его вдыхать. Таких людей называют «пассивными курильщиками». Курение особенно опасно для молодого и женского организмов.
Никотин относится к наркотическим веществам.
Наркотиком является и морфин — первый алкалоид, полученный химиками из растений. Он содержится в соке опийного мака. Это белое кристаллическое вещество, малорастворимое в воде и спирте. Оно обладает обезболивающим и снотворным действием, вызывает состояние эйфории.
Опасность наркотиков для жизни. Наркотические вещества сильно влияют на центральную нервную систему. Человек легко привыкает к их употреблению, попадает в устойчивую психическую и физическую зависимость от этих веществ, постепенно деградирует как личность, а потом погибает. Это — трагедия как для самого наркомана, так и для его родных и друзей.
Это интересно: Существуют наркотики, зависимость от которых возникает после одного-двух приемов.
Современная медицина может избавить человека от привычки употреблять наркотики. Но очень важным является наличие у человека сильного желания возвратиться к здоровому образу жизни.
Выводы:
- Физиологически активные вещества — соединения, активно влияющие на биологические процессы в живых организмах. Некоторые из них содержатся в растениях, организмах животных, а другие получают в лабораториях.
- Физиологически активными веществами являются витамины, алкалоиды, антибиотики, гормоны.
- Витамины — органические соединения, необходимые организму в незначительных количествах для осуществления важных биохимических процессов. Витамины делят на водорастворимые и жирорастворимые.
- Алкалоиды — нитрогенсодержащие органические соединения, оказывающие сильное физиологическое действие на организмы животных и человека. Они содержатся в чае, кофе, какао, табаке. Некоторые алкалоиды являются наркотиками. Человек легко привыкает к их употреблению и тем самым наносит серьезный вред своему организму.
| Рекомендую подробно изучить предметы: |
| Ещё лекции с примерами решения и объяснением: |