
Кислород как химический элемент в химии - формулы, определение с примерами
Содержание:
Кислород как химический элемент:
Кислород — самый распространенный элемент на Земле.
Дыхание, горение, многие процессы в живой и неживой природе, а также в технике протекают в присутствии кислорода как простого вещества.
Кислород, являясь самым распространенным элементом в земной коре, считается одним из самых необходимых элементов для жизнедеятельности на Земле.
Кислород был открыт в 1774 г. Дж. Пристли и независимо от него — К. Шееле, но как новое вещество его подробно охарактеризовал А. Лавуазье.
Название «кислород» предложено А. Лавуазье. По-латыни (oxygenium) оно означает «рождающий кислоты». Химическим знаком его была взята первая буква латинского названия. Порядковый номер кислорода в периодической системе — 8, а относительная атомная масса равна 15,9994 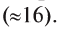
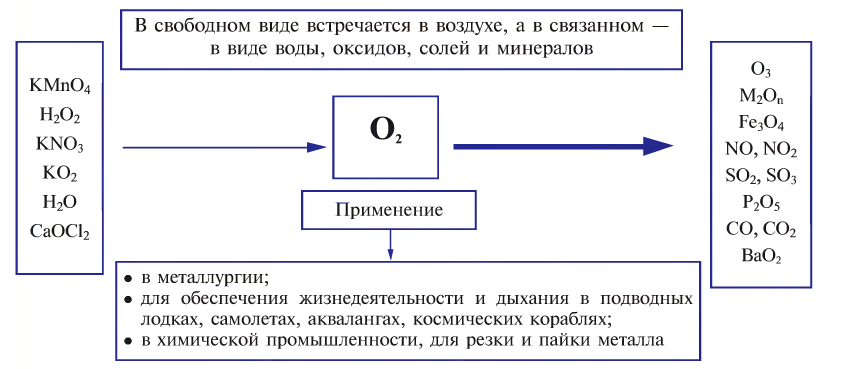
В свободном виде кислород встречается в атмосферном воздухе, а в связанном виде, т.е. в виде соединений, входит в состав воды, минералов и других веществ, составляющих горные породы, а также растительные и животные организмы. В земной коре масса кислорода составляет 47%. Объемная доля молекулярного кислорода в воздухе составляет 20,94%. В воде масса связанного кислорода составляет 89%.
- Химический знак кислорода — О.
- Формула простого вещества —
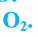
- Относительная атомная масса

- Относительная молекулярная масса

- Валентность в соединениях — 2.
- Эквивалентная масса — 8 г/моль.
- Эквивалентный объем — 5,6 л/моль.
Кислород как простое вещество
Получение:
В лаборатории кислород получают следующими способами.
1. Термическим разложением перманганата калия:
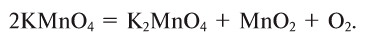
2. Термическим разложением бертолетовой соли в присутствии катализатора:
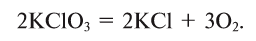
3. Термическим разложением нитратов щелочных металлов:
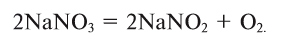
4. Электролизом воды (рис. 19):
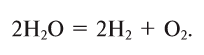

Рис. 19. При электролизе воды образуется один объем кислорода и два объема 4
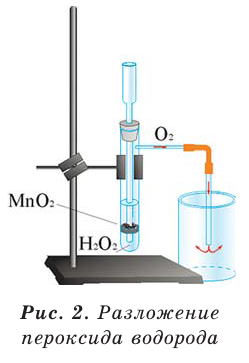
5. Пероксид водорода в присутствии катализатора оксида марганца (IV) разлагается на воду и кислород (рис. 20):
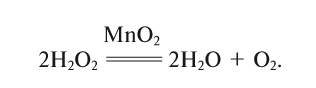
В промышленности кислород получают электролизом воды или из жидкого воздуха.
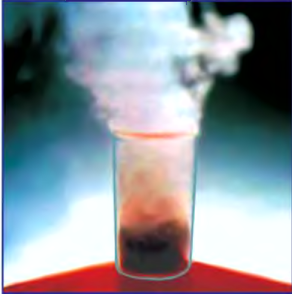
Рис. 20. Разложение 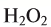 присутствии
присутствии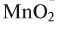
Понятие о катализаторах:
Если обратить внимание на реакцию получения кислорода посредством разложения пероксида водорода, то можно увидеть, что этот процесс осуществляется очень быстро в присутствии черного порошка — оксида марганца (IV) — 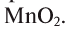 . Кислород начинает интенсивно выделяться, и после реакции в сосуде остаются вода и неизрасходованный порошок.
. Кислород начинает интенсивно выделяться, и после реакции в сосуде остаются вода и неизрасходованный порошок.
Если отделить фильтрованием порошок, находящийся на дне сосуда, и высушить его, то можно заметить, что его исходные масса и свойства не изменились. Им можно пользоваться при разложении других образцов пероксида водорода.
Вещества, участвующие в химической реакции и ускоряющие ее, но которые при этом не расходуются и не изменяются, называются катализаторами.
Процесс, протекающий в присутствии катализатора, называется катализом.

Рис. 21. Притяжение кислорода к магниту
Физические свойства:
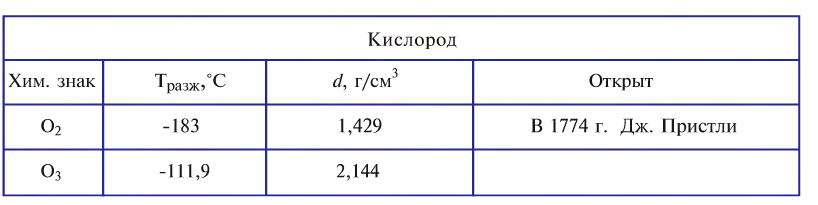
Молекула кислорода состоит из двух атомов и как простое вещество выражается формулой 02. Относительная молекулярная масса равна 32. При обычных условиях кислород — газ без цвета, вкуса и запаха. Он немного тяжелее воздуха (1 л кислорода весит 1,43 г, а 1 л воздуха — 1,293 г). Кислород мало растворяется в воде: при 0°С в 1 л — 49 мл кислорода, при 20°С в 1л — 31 мл кислорода. Приблизительно при 1500°С кислород расщепляется на атомы. При —183°С кислород превращается в голубоватую жидкость. Жидкий кислород способен притягиваться к магниту (рис. 21).
Озон:
При пропускании через кислород или воздух электрической искры (или грозового разряда) образуется новое вещество с характерным запахом — озон. Возможность получения озона из чистого кислорода доказывает, что он является его аллотропическим видоизменением и состоит из атомов кислорода:
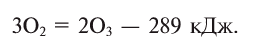
Озон постоянно образуется в стратосфере (слой атмосферы на высоте 23—25 км от Земли) под действием ультрафиолетовых лучей, а также в результате окисления смолистых веществ хвойных растений. Озоновый слой составляет в толщину 2—4,5 мм, он защищает Землю от губительной солнечной радиации (вредных лучей). Нарушение целостности озонового слоя чрезвычайно опасно для жизни на Земле. Поэтому ученые постоянно проводят исследования по изучению причин появления озоновых дыр и мер по их предупреждению.
Озон разъедает резину, обесцвечивает масло и бумагу, убивает бактерии. Он используется при усовершенствовании технологических процессов в промышленности, при очистке дымовых газов, промышленных и бытовых стоков, а также при дезинфекции питьевой воды.
Озон — газ голубого цвета с характерным запахом, в воде растворяется лучше, чем кислород (при 0°С в 1 л воды 490 мл).
Озон легко разлагается: 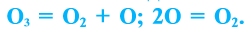
В лаборатории озон получают с помощью озонатора.
Озон отделяют от кислорода путем сильного вымораживания (озон кипит при температуре -111,9°С).
Озон ядовит. Его количество в воздухе не должно превышать 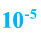 %.
%.
Серебро не взаимодействует с кислородом, но при взаимодействии с озоном дает оксид.
Химические свойства кислорода:
Кислород (после фтора) — самый активный неметалл.
Кислород поддерживает горение.
Кислород соединяется почти со всеми металлами (окисляет их), кроме золота, серебра, платины и металлов группы платины:
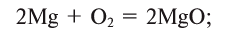
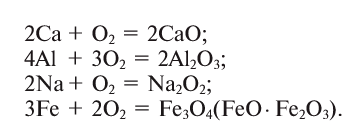
Кислород вступает в реакцию также со всеми неметаллами, кроме галогенов (элементов VII группы главной подгруппы), образуя оксиды:
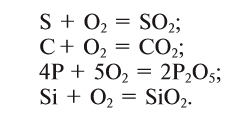
Кислород также вступает в реакцию со сложными органическими и неорганическими веществами:
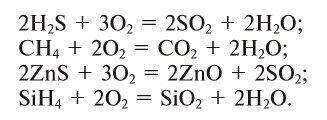
Оксиды — это вещества, образующиеся в результате взаимодействия кислорода и большинства простых или сложных веществ.
В оксидах кислород двухвалентен.
Биологическое значение кислорода
Кислород считается важным биогенным элементом. Он составляет 45% сухой биомассы растений. Процесс дыхания живых организмов на Земле непосредственно связан с кислородом. Кислород также является источником озонового слоя, задерживающего опасные солнечные лучи. Роль кислорода огромна при распаде и гниении умерших организмов. Процесс фотосинтеза также нельзя представить без кислорода. Он составляет 65% тела человека.
Применение кислорода
Кислород широко применяется в медицине, при обеспечении жизнедеятельности в подводных и космических аппаратах, при осуществлении процессов дыхания, горения и гниения, для создания высоких температур в производственных процессах, в производстве химических веществ, в качестве окислителя топлива в различных агрегатах. Кислород хранится в 40-литровых голубых баллонах (вес тары 80 кг) при давлении 150-160 атм и объеме 6-7 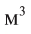 (вес кислорода 9—10 кг) и выставляется на продажу для технических целей.
(вес кислорода 9—10 кг) и выставляется на продажу для технических целей.
Круговорот кислорода в природе
О том, что кислород в большом количестве находится в литосфере, гидросфере и атмосфере, мы говорили в предыдущих разделах учебника (табл. 5).

Круговорот кислорода на Земле несущественно отличается от его круговорота в атмосфере, литосфере и гидросфере. На Земле круговорот в основном протекает в процессе фотосинтеза и дыхания. В процессе фотосинтеза углекислый газ, взаимодействуя с водой, образует органические вещества и кислород. В результате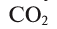 расходуется на образование биомассы. При этом кислород, входящий в состав воды в виде 02, полностью переходит в атмосферу. Таким образом, фотосинтез обеспечивает переход кислорода из гидросферы в атмосферу, а затем в биосферу (выделение кислорода из молекулы воды обозначено знаком *):
расходуется на образование биомассы. При этом кислород, входящий в состав воды в виде 02, полностью переходит в атмосферу. Таким образом, фотосинтез обеспечивает переход кислорода из гидросферы в атмосферу, а затем в биосферу (выделение кислорода из молекулы воды обозначено знаком *):
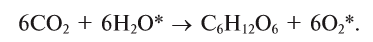
При дыхании, разложении умерших организмов и горении кислород из биосферы возвращается обратно в гидросферу и атмосферу:
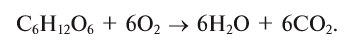
В биомассе Земли кислород полностью меняется каждые 20—30 лет. В литосферу кислород переходит из атмосферы в виде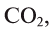 , который связывается и превращается в
, который связывается и превращается в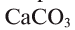 (например, в раковинах моллюсков), а затем эти карбонаты при термическом разложении образуют углекислый газ, который возвращается в атмосферу:
(например, в раковинах моллюсков), а затем эти карбонаты при термическом разложении образуют углекислый газ, который возвращается в атмосферу: 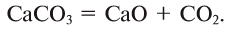
Эта реакция наблюдается в основном в зонах повышенной вулканической деятельности, тем самым постепенно обновляя углекислый газ в атмосфере.
Кислород и воздух
Атмосферный воздух — это природная смесь многих газов. Помимо азота и кислорода, являющихся основной составной частью воздуха, в его состав входят в небольшом количестве инертные газы, углекислый газ, пары воды и водород (табл. 6). Кроме них, в воздухе встречаются, в зависимости от внешних условий, пыль, некоторые случайные примеси. Кислород, азот и инертные газы являются постоянными составляющими воздуха, они встречаются в любом месте почти в одинаковом количестве. Содержание же углекислого газа, паров воды и пыли изменяется в зависимости от условий.
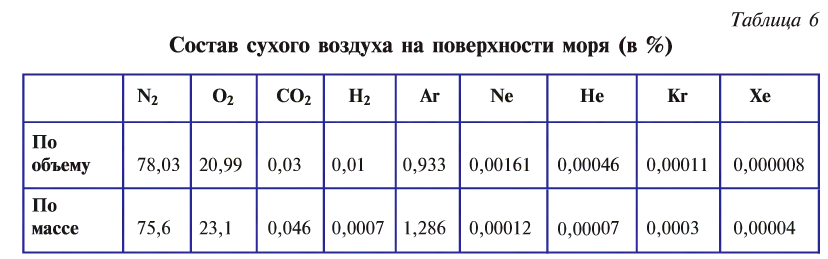
Один литр воздуха при 20°С и нормальном атмосферном давлении весит 1,293 г. При —192°С и давлении 101,33 кПа воздух превращается в бесцветную прозрачную жидкость. Из жидкого воздуха выделяются азот, кислород и инертные газы.
Углекислый газ и водяные пары воздуха выполняют функцию защитного экрана, препятствующего распространению во Вселенной тепла Земли, а озон не пропускает губительные для жизни на Земле коротковолновые ультрафиолетовые лучи, исходящие от Солнца и звезд. Твердые частицы воздуха (пыль) служат основой для образования дождевых капель (в состав пыли входят минеральные вещества, частицы угля, растительная пыль и различные бактерии).
К случайным примесям воздуха относятся сероводород и аммиак, образующиеся при гниении органических остатков, выбрасываемый промышленными предприятиями сернистый газ, образующиеся в результате электрических разрядов оксиды азота, которые периодически выводятся из состава воздуха дождем и снегом.
Воздух является необходимой составной частью жизни на Земле. Сохранение его чистоты имеет огромное значение для человечества. Для защиты воздуха от техногенных загрязнений необходимо использовать новые безотходные технологии, предупреждать уменьшение биомассы Земли, обеспечивать нормальную работу естественных механизмов очистки воздуха.
Горение и виды горючих веществ
Реакция, протекающая с участием кислорода и сопровождающаяся выделением большого количества света и тепла, называется горением.
В чистом кислороде, по сравнению с воздухом, вещества горят во много раз быстрее (рис. 22). В обоих случаях выделяется равное количество теплоты, но в кислороде этот процесс протекает быстрее и выделяющаяся теплота не расходуется, как в случае с воздухом, на нагревание азота. Температура при горении в чистом кислороде выше, чем в воздухе. Опуская тлеющую лучину в сосуд с чистым кислородом, можно увидеть, как она сразу загорается. А в воздухе тлеющая лучина может вскоре и потухнуть. Если эта лучина зажжена, то она продолжает гореть на воздухе, потому что выделяющееся при горении тепло требует большей температуры, чем температура воспламенения лучины.

Рис. 22. Горение магния в чистом кислороде

Рис. 23. Тушение пламени
Температура, необходимая для поджигания вещества на воздухе, называегся температурой воспламенения.
Значит, для обеспечения горения веществ, нужно нагревать их до температуры воспламенения и подавать кислород в достаточном количестве.
Для того чтобы потушить пламя, необходимо ликвидировать факторы, обеспечивающие его появление, т.е. охладить вещество до температуры ниже температуры возгорания и прекратить подачу кислорода (рис. 23).
Чтобы потушить горящую вещь, сначала следует понизить температуру, используя невоспламеняющиеся средства, затем накрыть источник возгорания одеялом или брезентом, чтобы прекратить подачу воздуха.
В непредвиденных ситуациях для тушения пожара необходимо использовать специальные средства, а если их нет, то применять указанный выше способ.
Вообще процесс горения имеет огромное значение в промышленности и в повседневной жизни.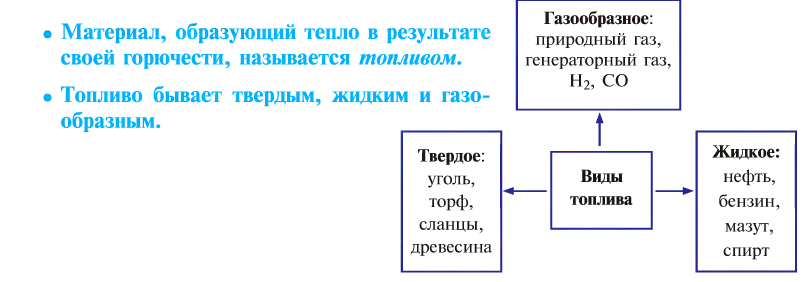
От твердого топлива остается минеральный осадок — пепел. Жидкое и газообразное топливо такого недостатка не имеет. Но любое топливо независимо от места добычи, промышленного объема, экономической эффективности имеет только свое место применения, и возможности по его взаимозамещению ограничены.
Неправильное сжигание топлива приносит вред народному хозяйству.
Топливо позволяет спокойно переносить холод, варить пищу, которая не употребляется в сыром виде, получать металлы из руд путем их выплавки, обеспечивать движение транспорта, получать другие виды энергии.
Оксиген
Это первый элемент, который вы будете подробно изучать. Из периодической системы Д. И. Менделеева можно получить такие сведения о нем:
- • символ Оксигена — О;
- • порядковый номер элемента — 8;
- • Оксиген находится во 2-м периоде, в VI группе;
- • относительная атомная масса элемента — 16 (точное значение — 15,999).
Значение порядкового номера элемента указывает на то, что атом Оксигена содержит 8 электронов, а заряд ядра атома равен +8.
Оксиген — неметаллический элемент, поскольку его простые вещества кислород 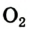 и озон
и озон 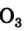 являются неметаллами.
являются неметаллами.
Вам известно, что Оксиген имеет постоянное значение валентности — 2. Атом этого элемента легко присоединяет 2 электрона и превращается в простой ион 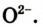 .Такие ионы содержатся в бинарных соединениях Оксигена с металлическими элементами.
.Такие ионы содержатся в бинарных соединениях Оксигена с металлическими элементами.
Распространенность оксигена в природе
Оксиген — один из самых распространенных элементов на нашей планете. В земной коре его атомов больше, чем атомов любого другого элемента (§ 6). Атомы Оксигена содержатся в песке, глине, известняке, многих минералах. Оксиген — второй по распространенности в атмосфере (после Нитрогена) и в гидросфере (после Гидрогена).
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 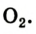 Это вещество содержит молекулы, состоящие из двух атомов Оксигена.
Это вещество содержит молекулы, состоящие из двух атомов Оксигена.
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
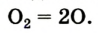
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5
Атомы Оксигена входят в состав молекул многих веществ, находящихся в живых организмах (белков, жиров, крахмала и пр.). В теле взрослого человека массовая доля этого элемента составляет примерно 65 %.
Кислород. Важнейшее простое вещество Оксигена — кислород. Этот газ необходим для дыхания; он поддерживает горение.
Формула кислорода вам известна — 02. Это вещество содержит молекулы, состоящие из двух атомов Оксигена.
Молекула кислорода достаточно устойчива. Но под действием электрического разряда или ультрафиолетовых лучей, а также при температуре свыше 2000 °С она распадается на атомы:
02 = 20.
Кислород — компонент воздуха, природной смеси газов. На него приходится приблизительно 1/5 объема воздуха. Состав сухого воздуха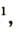 не содержащего случайных примесей, приведен в таблице.
не содержащего случайных примесей, приведен в таблице.
Организм взрослого мужчины ежесуточно потребляет приблизительно 900 г кислорода, а женщины — 600 г.
Состав воздуха:
Газ компонент воздуха Доля воздуха в%
| Название | Формула | объемная* | массовая |
Азот |
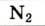 |
78,09 | 75,51 |
| Кислород | 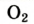 |
20,95 | 23,15 |
| Аргон | 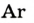 |
0,93 | 1,28 |
| углекислый газ | 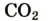 |
0,037 | 0,056 |
| Другие газы | менее 0,002 | менее 0,003 |
* Объемная доля вещества в смеси — отношение объема вещества к объему смеси. Объемную долю обозначают греческой буквой 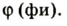
Определить объемную долю кислорода в воздухе можно экспериментально. Для этого нужны стеклянная бутылка без дна с пробкой и кристаллизатор с водой. В пробку вставляют ложку для сжигания, в которую набрано немного красного фосфора. Его поджигают, быстро вносят в бутылку и плотно I закрывают ее пробкой (рис. 52). Когда горение фосфора прекратится, вода займет примерно 1/5 часть объема бутылки. Этот объем занимал в воздухе кислород, который вступил в реакцию с фосфором.
Кислород содержится не только в атмосфере. Небольшое его количество вместе с другими газами воздуха растворено в природной воде.
Существует еще одно простое вещество Оксигена — озон 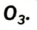 Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород:
Это бесцветный сильнотоксичный газ с резким запахом. Он очень неустойчив и постепенно превращается в кислород: 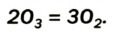
Озон содержится в атмосфере в незначительном количестве; его объемная доля не превышает
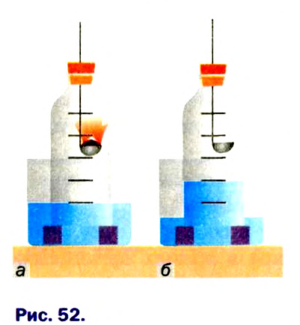
Определение объемной доли кислорода в воздухе сжиганием фосфора:
а — начало опыта;
б — окончание опыта
 Воздух содержит еще и примесь водяного пара, обусловливающего его влажность.
Воздух содержит еще и примесь водяного пара, обусловливающего его влажность.
1 0,0004 %. Распадаясь, он поглощает часть ультрафиолетовых лучей солнечного света, вредную для растений и животных, и тем самым оберегает природу.
Физические свойства кислорода
В обычных условиях кислород — бесцветный газ, который не имеет запаха и вкуса. При охлаждении до -183 °С превращается в голубую жидкость, которая при температуре -219 °С затвердевает, образуя синие кристаллы. Кислород в 1,1 раза тяжелее воздуха. Он плохо растворяется в воде, но этого достаточно для существования в природных водоемах рыб, других живых существ, которые дышат растворенным кислородом.
Жидкий кислород, как и железо, притягивается к магниту.
Вывод:
Оксиген — неметаллический элемент. В природе распространено его простое вещество кислород, а также вода и другие соединения. На кислород приходится немногим более 1/5 объема воздуха.Кислород — газ без запаха и вкуса, необходимый для дыхания; он поддерживает горение.
Открытие кислорода
Кислород был открыт во второй половине XVIII в. несколькими учеными разных стран. Первым этот газ получил шведский химик К.-В. Шееле в 1772 г., а через два года, не зная об опытах предшественника, — английский химик Дж. Пристли. В 1775 г. французский ученый A.-JI. Лавуазье исследовал кислород и дал ему название oxygen.
Кислород можно обнаружить с помощью тлеющей лучинки. Лучинка, помещенная в сосуд с этим газом, ярко вспыхивает (рис. 53).

Рис. 53.Обнаружение кислорода:
а — тлеющая лучинка на воздухе; б — возгорание лучинки в кислороде
Получение кислорода в промышленности
Неисчерпаемым источником кислорода является воздух. Чтобы получить из него кислород, следует отделить этот газ от азота и других газов. На такой идее основан промышленный метод получения кислорода. Его реализуют, используя специальную, достаточно громоздкую аппаратуру. Сначала воздух сильно охлаждают до превращения его в жидкость. Затем температуру сжиженного воздуха постепенно повышают. Первым из него начинает выделяться газ азот (температура кипения жидкого азота составляет -196 °С), а жидкость обогащается кислородом (температура кипения кислорода -183 °С).
Получение кислорода в лаборатории
Лабораторные методы получения кислорода основаны на химических реакциях.
Дж. Пристли получал этот газ из соединения, название которого — меркурий оксид. Ученый использовал стеклянную линзу, с помощью которой фокусировал на веществе солнечный свет.
оксид. Ученый использовал стеклянную линзу, с помощью которой фокусировал на веществе солнечный свет.
В современном исполнении этот опыт изображен на рисунке 54. При нагревании меркурий оксид (порошок желтого цвета) превращается в ртуть и кислород. Ртуть выделяется в газообразном состоянии и конденсируется на стенках пробирки в виде серебристых капель. Кислород собирается над водой во второй пробирке.
оксид (порошок желтого цвета) превращается в ртуть и кислород. Ртуть выделяется в газообразном состоянии и конденсируется на стенках пробирки в виде серебристых капель. Кислород собирается над водой во второй пробирке.
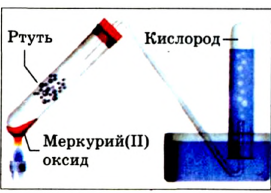
Рис. 54.Получение кислорода нагреванием меркурий оксида
оксида
Соответствующее химическое уравнение:
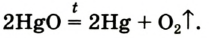
Сейчас метод Пристли не используют, поскольку пары ртути токсичны. Кислород получают с помощью других реакций, подобных рассмотренной. Они, как правило, происходят при нагревании.
Реакции, при которых из одного вещества образуются несколько других, называют реакциями разложения.
Для получения кислорода в лаборатории используют такие оксигенсодержащие соединения:
- калий перманганат
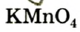 (бытовое название — марганцовка; вещество является распространенным дезинфицирующим средством)
(бытовое название — марганцовка; вещество является распространенным дезинфицирующим средством)
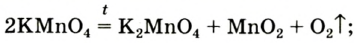
- калий хлорат
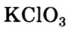 (тривиальное название — бертолетова соль, в честь французского химика конца XVIII — начала XIX в. K.-Л. Бертолле)
(тривиальное название — бертолетова соль, в честь французского химика конца XVIII — начала XIX в. K.-Л. Бертолле)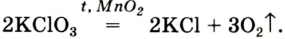
Небольшое количество катализатора — манган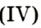 оксида
оксида 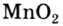 — добавляют к калий хлорату для того, чтобы разложение соединения происходило с выделением кислорода
— добавляют к калий хлорату для того, чтобы разложение соединения происходило с выделением кислорода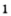 .
.
Получение кислорода разложением гидроген пероксида 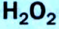
Налейте в пробирку 2 мл раствора гидроген пероксида (традиционное название этого вещества — перекись водорода). Зажгите длинную лучинку и погасите ее (как вы это делаете со спичкой), чтобы она едва тлела. Насыпьте в пробирку с раствором гидроген пероксида немного катализатора — черного порошка манган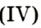 оксида. Наблюдайте бурное выделение газа. С помощью тлеющей лучинки убедитесь в том, что этот газ — кислород.
оксида. Наблюдайте бурное выделение газа. С помощью тлеющей лучинки убедитесь в том, что этот газ — кислород.
Составьте уравнение реакции разложения гидроген пероксида, если вторым продуктом реакции является вода
В лаборатории кислород можно также получить разложением натрий нитрата 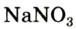 или калий нитрата
или калий нитрата  Соединения при нагревании сначала плавятся, а затем разлагаются:
Соединения при нагревании сначала плавятся, а затем разлагаются:
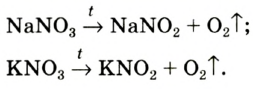
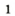 При нагревании соединения без катализатора происходит другая реакция:
При нагревании соединения без катализатора происходит другая реакция: 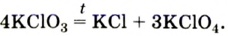
 Эти вещества используют в качестве удобрений. Их общее название — селитры.
Эти вещества используют в качестве удобрений. Их общее название — селитры.
Кислород вместе с водородом являются продуктами разложения воды под действием электрического тока: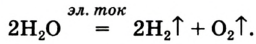
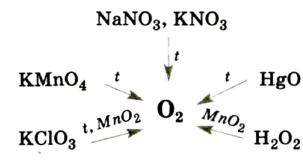
Лабораторные методы получения кислорода
В природе кислород образуется вследствие фотосинтеза в зеленых листьях растений. Упрощенная схема этого процесса такова:
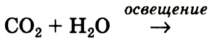 органические вещества (глюкоза,крахмал и др.)+
органические вещества (глюкоза,крахмал и др.)+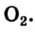
Выводы:
Кислород был открыт в конце XVIII в. несколькими учеными. Кислород получают в промышленности из воздуха, а в лаборатории — с помощью реакций разложения некоторых оксигенсодержащих соединений. Во время реакции разложения из одного вещества образуются два или более веществ.
Химические свойства кислорода
Химические свойства каждого вещества проявляются в химических реакциях при его участии.
Кислород — один из наиболее активных неметаллов. Но в обычных условиях он реагирует с немногими веществами. Его реакционная способность существенно возрастает с повышением температуры.
Реакции кислорода с простыми веществами
Кислород реагирует, как правило, при нагревании, с большинством неметаллов и почти со всеми металлами.
Реакция с углем (углеродом)
Известно, что уголь, нагретый на воздухе до высокой температуры, загорается. Это свидетельствует о протекании химической реакции вещества с кислородом. Теплоту, которая выделяется при этом, используют, например, для обогрева домов в сельской местности.
Основным продуктом сгорания угля является углекислый газ. Его химическая формула —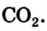 Уголь — смесь многих веществ. Массовая доля Карбона в нем превышает 80 %. Считая, что уголь состоит только из атомов Карбона, напишем соответствующее химическое уравнение:
Уголь — смесь многих веществ. Массовая доля Карбона в нем превышает 80 %. Считая, что уголь состоит только из атомов Карбона, напишем соответствующее химическое уравнение:
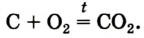
Карбон образует простые вещества — графит и алмаз. Они имеют общее название — углерод — и взаимодействуют с кислородом при нагревании согласно приведенному химическому уравнению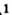 .
.
Реакции, при которых из нескольких веществ образуется одно, называют реакциями соединения.
Реакция с серой
Это химическое превращение осуществляет каждый, когда зажигает спичку; сера входит в состав ее головки. В лаборатории реакцию серы с кислородом проводят в вытяжном шкафу. Небольшое количество серы (светло-желтый порошок или кристаллы) нагревают в железной ложке. Вещество сначала плавится, потом загорается в результате взаимодействия с кислородом воздуха и горит едва заметным синим пламенем (рис. 56, б). Появляется резкий запах продукта реакции — сернистого газа (этот запах мы ощущаем в момент загорания спички). Химическая формула сернистого газа — 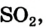 а уравнение реакции —
а уравнение реакции — 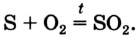

Рис. 56. Сера (а) и ее горение на воздухе (б) и в кислороде (в)
 В случае недостаточного количества кислорода образуется другое соединение Карбона с Оксигеном — угарный газ
В случае недостаточного количества кислорода образуется другое соединение Карбона с Оксигеном — угарный газ 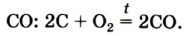
Если ложку с горящей серой поместить в сосуд с кислородом, то сера будет гореть более ярким пламенем, чем на воздухе (рис. 56, в). Это можно объяснить тем, что молекул 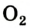 в чистом кислороде больше, чем в воздухе.
в чистом кислороде больше, чем в воздухе.


Рис. 57.Красный фосфор (а) и его горение на воздухе (б) и в кислороде (в)
Реакция с фосфором
Фосфор, как и сера, горит в кислороде интенсивнее, чем на воздухе (рис. 57). Продуктом реакции является белое твердое вещество — фосфор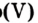 оксид (его мелкие частицы образуют дым):
оксид (его мелкие частицы образуют дым):
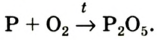
Реакция с магнием. Раньше эту реакцию использовали фотографы для создания яркого освещения («магниевая вспышка») при фотосъемке. В химической лаборатории соответствующий опыт проводят так. Металлическим пинцетом берут магниевую ленту и поджигают на воздухе. Магний сгорает ослепительно-белым пламенем (рис. 58, б); смотреть на него нельзя! В результате реакции образуется белое твердое вещество. Это соединение Магния с Оксигеном; его название — магний оксид.

Рис. 58. Магний (а) и его горение на воздухе (б)
Реакции кислорода со сложными веществами
Кислород может взаимодействовать с некоторыми оксигенсодержащими соединениями. Например, угарный газ СО горит на воздухе с образованием углекислого газа:
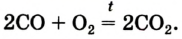
Немало реакций кислорода со сложными веществами мы осуществляем в повседневной жизни, сжигая природный газ (метан), спирт, древесину, бумагу, керосин и др. При их горении образуются углекислый газ и водяной пар:
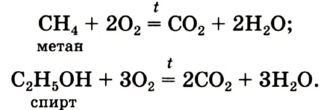
Оксиды
Продуктами всех реакций, рассмотренных в параграфе, являются бинарные соединения элементов с Оксигеном.
Соединение, образованное двумя элементами, одним из которых является Оксиген, называют оксидом.
Общая формула оксидов — 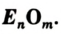
Каждый оксид имеет химическое название, а некоторые — еще и традиционные, или тривиальные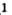 , названия (табл. 4). Химическое название оксида состоит из двух слов. Первым словом является название соответствующего элемента, а вторым — слово «оксид». Если элемент имеет переменную валентность, то он может образовывать несколько оксидов. Их названия должны отличаться. Для этого после названия элемента указывают (без отступа) римской цифрой в скобках значение его валентности в оксиде. Пример такого названия соединения: купрум
, названия (табл. 4). Химическое название оксида состоит из двух слов. Первым словом является название соответствующего элемента, а вторым — слово «оксид». Если элемент имеет переменную валентность, то он может образовывать несколько оксидов. Их названия должны отличаться. Для этого после названия элемента указывают (без отступа) римской цифрой в скобках значение его валентности в оксиде. Пример такого названия соединения: купрум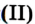 оксид (читается «купрум-два-оксид»).
оксид (читается «купрум-два-оксид»).
Таблица 4
Формулы и названия некоторых оксидов
| Формула | Название | |
|---|---|---|
| традиционное (тривиальное) | химическое | |
| СаО | Негашеная известь | Кальций оксид |
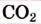 |
Углекислый газ | Карбон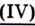 оксид оксид |
| СО | Угарный газ | Карбон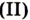 оксид оксид |
 Термин происходит от латинского слова trivialis — обыкновенный.
Термин происходит от латинского слова trivialis — обыкновенный.
Выводы:
Кислород — химически активное вещество. Он взаимодействует с большинством простых веществ, а также со сложными веществами. Продуктами таких реакций являются соединения элементов с Оксигеном — оксиды.
Реакции, при которых из нескольких веществ образуется одно, называют реакциями соединения.
Горение и кислород
Рассмотренные в предыдущем параграфе реакции с участием кислорода сопровождаются одинаковыми внешними эффектами.
Химическую реакцию, во время которой выделяется теплота и появляется пламя, называют горением.
Пламя возникает вследствие свечения раскаленных частиц веществ, которые сгорают или образуются во время реакции.
Для того чтобы горючее вещество воспламенилось, необходимы такие условия:
- наличие кислорода (воздуха);
- нагревание вещества до температуры самовозгорания (для бензина она составляет 220 °С, сухой древесины — 250—300 °С, бумаги — 440 °С, угля — свыше 600 °С).
Кислород поддерживает горение веществ, но сам не горит.
Если не выполняется хотя бы одно из этих условий, то горение не происходит. Это учитывают во время работы с огнеопасными веществами, а также при тушении пожаров.
Погасить огонь можно, залив горящее вещество или предмет водой, засыпав его песком или землей, накрыв одеялом или направив на него струю углекислого газа (он не поддерживает горения и тяжелее воздуха) (рис. 63).


Рис. 63. Гашение пламени:
а — водой; б — песком; в — углекислым газом
В лабораториях, на предприятиях с этой целью используют огнетушители (рис. 64).


Рис. 64. Огнетушитель (а)и его использование (б)
Окисление и кислород
Взаимодействие веществ с кислородом не всегда сопровождается их горением. Большинство таких реакций происходят медленно, иногда — незаметно. Вещество, которое взаимодействует с кислородом, подвергается окислению, т. е. изменяется при участии кислорода.
Медленным окислением веществ обусловлено появление ржавчины на железе, прокисание молока, прогорание масла, порча многих других продуктов питания.
Реакции веществ с кислородом, которые не сопровождаются горением, используют в цветной металлургии, химической промышленности.
Кислород, поступая через легкие в организм животного или человека, окисляет различные вещества, в том числе и те, которые постоянно поступают вместе с пищей.
Выводы:
При взаимодействии некоторых веществ с кислородом происходит их горение — химическое превращение с выделением теплоты и появлением пламени.
Условиями, необходимыми для горения, являются наличие кислорода и достижение веществом определенной температуры. Для того чтобы погасить пламя, необходимо устранить хотя бы одно из этих условий.
Любую реакцию вещества с кислородом называют окислением. Многие из таких реакций происходят медленно и не сопровождаются появлением пламени.
Круговорот оксигена в природе
Каждое мгновение на Земле происходит множество физических и химических превращений. Эти изменения в природе являются циклическими, т. е. периодически повторяющимися.
Часть изменений, которые происходят с веществами на планете, обусловлена химическими реакциями.
Совокупность процессов, происходящих в природе, при которых атомы или ионы элемента в результате реакций переходят от одних веществ к другим, называют круговоротом элемента.
Если главным веществом в круговороте Оксигена выбрать кислород, то можно выделить такие звенья круговорота (схема 8):
- расходование, или связывание, кислорода (процессы дыхания, сгорания топлива и горючего, окисление различных веществ в природе, в технологических процессах);
- взаимопревращение оксигенсодержащих соединений;
- образование кислорода (процесс фотосинтеза, разложение воды в верхних слоях атмосферы). Неизменность содержания кислорода в атмосфере свидетельствует о том, что процессы связывания и выделения кислорода компенсируют друг друга.
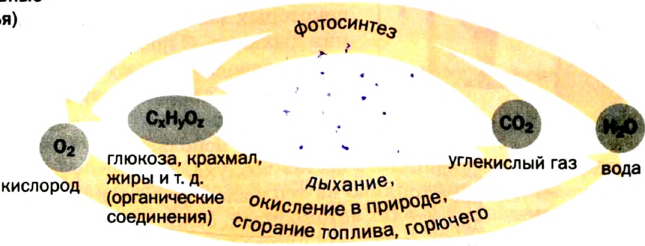
Схема 8. Круговорот Оксигена(основные звенья)
Оксиген способствует круговороту других элементов, поскольку образует с ними многочисленные соединения.
Применение кислорода в различных отраслях
Кислород используют в различных отраслях, причем в больших количествах (схема 9). В металлургии он ускоряет процесс выплавки стали и улучшает ее качество. Этот газ необходим в производстве многих химических соединений, используется в специальных устройствах для резки и сварки металлов (водородно-кислородные, ацетиленово-кислородные горелки). Баллоны, наполненные кислородом (рис. 66) или его смесью с инертным газом гелием, используют космонавты, военные летчики, пожарники, водолазы. Кислородные подушки применяют при некоторых заболеваниях для облегчения дыхания. С помощью сжиженного кислорода создают необходимые условия для сгорания горючего в космических ракетах.

Схема 9.Применение кислорода
Широко используется и кислород, входящий в состав воздуха. При его участии сгорает топливо на теплоэлектростанциях, горючее в двигателях автомобилей, обжигают металлические руды на заводах цветной металлургии.
Рис. 66. Баллон с кислородом
Во время сжигания топлива и горючего образуется и попадает в воздух значительное количество угарного (СО) и сернистого 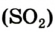 газов. Эти вещества негативно влияют на растения, вызывают и обостряют болезни у людей. Поэтому в каждой стране работу промышленности, энергетики, транспорта организуют так, чтобы уменьшить количество вредных выбросов в атмосферу. Охрана воздуха от техногенных загрязнений является важным государственным делом.
газов. Эти вещества негативно влияют на растения, вызывают и обостряют болезни у людей. Поэтому в каждой стране работу промышленности, энергетики, транспорта организуют так, чтобы уменьшить количество вредных выбросов в атмосферу. Охрана воздуха от техногенных загрязнений является важным государственным делом.
Биологическая роль кислорода
Кислород необходим живым существам для дыхания. Попадая через легкие в организм, этот газ соединяется с гемоглобином (компонент крови) и поступает во все органы и ткани. При участии кислорода происходят различные реакции. Некоторые из них сопровождаются выделением теплоты; благодаря этому поддерживается постоянная температура тела.
Выводы:
В природе атомы Оксигена в результате химических реакций постоянно переходят от одних веществ к другим; происходит круговорот этого элемента.
Кислород широко используется в промышленности, технике, медицине, а в составе воздуха — в теплоэнергетике, автотранспорте, других областях.
Кислород необходим живым существам. Попадая в организм во время дыхания, он принимает участие во многих химических реакциях. Кислород также является продуктом фотосинтеза.
Отравление угарным газом СО происходит потому, что он реагирует с гемоглобином, и поступление кислорода в организм прекращается.
Распространение кислорода в природе и его получение

Что происходит с вами, оставаясь в закрытом помещении, без воздуха? Какие газы и сколько процентов содержится в составе воздуха, которым мы дышим?
Общая характеристика:
- Химический знак: О
- Валентность: II
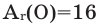
Химическая формула простого вещества: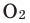
Относительная молекулярная масса простого вещества: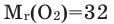
- Относительная атомная масса:

Распространение кислорода в природе:
Кислород был открыт в 1772 году шведским ученым Карлом Шееле. Это самый распространенный в природе элемент. Примерно 49,4% массы земной коры приходится на долю кислорода. Кислород в атмосфере земного шара (по массе 23%, по объёму 21%) и в природных водах существует в растворённом виде.
Наличие кислорода в атмосферном воздухе впервые было установлено А.Лавуазье в 1774 году. Кроме кислорода в воздухе содержится 78% по объему и 75,5% по массе азота (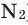 ) и примерно -1% инертных газов (аргона и др.), в минимальном количестве (-0,03%) - углекислого газа.
) и примерно -1% инертных газов (аргона и др.), в минимальном количестве (-0,03%) - углекислого газа.
Кислород в виде соединений является основной составной частью почвы, воды, горных пород, руд, минералов. Он входит в состав всех живых организмов (растений, животных и т.д.). Приблизительно 65% человеческого тела составляет элемент кислород.
В природных соединениях встречается три изотопа 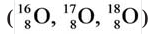 кислорода. Наиболее распространенным среди них является изотоп с относительной атомной массой 16.
кислорода. Наиболее распространенным среди них является изотоп с относительной атомной массой 16.

Французский химик. В 1774 году экспериментальным путем доказал состав воздуха.
Получение кислорода в лаборатории
Кислород получают в лаборатории в результате разложения воды под действием постоянного электрического тока:
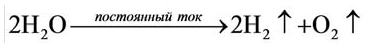
В результате разложения нитрата калия. Впервые кислород был открыт К.Шееле в 1772 году в результате реакции разложения нитрата калия.
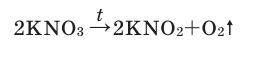
В результате разложения оксида ртути (II). В 1774 году кислород был получен английским ученым Джозефом Пристли путем нагревания оксида ртути (II) 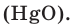 Однако, поскольку ртуть и её соединения являются ядовитыми, этим методом не пользуются.
Однако, поскольку ртуть и её соединения являются ядовитыми, этим методом не пользуются.
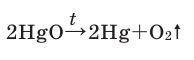
В настоящее время самыми удобными для получения кислорода в лабораторных условиях веществами являются известный в народе под названием «марганцовка» перманганат калия (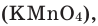 хлорат калия
хлорат калия 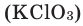 (Бертолетова соль) и пероксид водорода
(Бертолетова соль) и пероксид водорода 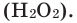
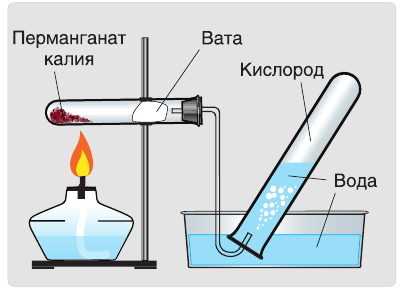
В результате разложения перманганата калия (рис. 1).
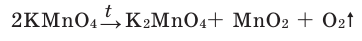
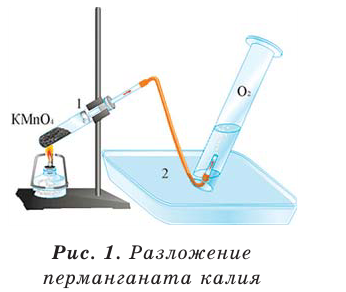
В результате разложения пероксида водорода 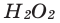 при участии оксида марганца (IV) (рис. 2).
при участии оксида марганца (IV) (рис. 2).
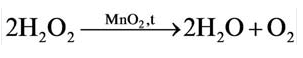
Вещества, которые ускоряют ход химических реакций, сохраняя при этом свое количество после реакции без изменения, называются катализаторами.
В результате разложения хлората калия (Бертолетова соль) при участии оксида марганца (IV) (рис. 3).
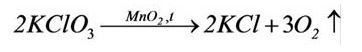
Без участия оксида марганца (IV) 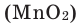 реакция протекает очень медленно.
реакция протекает очень медленно.  является катализатором в разложении пероксида водорода и хлората калия.
является катализатором в разложении пероксида водорода и хлората калия.
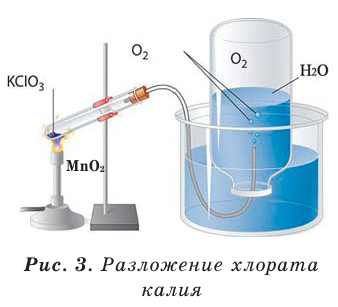
Получение кислорода в промышленности
В промышленности кислород в большом количестве получают при дистилляции сжиженного воздуха. Очистив воздух от пыли, влаги и углекислого газа, его сжижают путем сжатия под высоким давлением и охлаждения. Температуру сжиженного и охлажденного до - 200  С воздуха постепенно поднимают. Вначале испаряется азот (при температуре - 196
С воздуха постепенно поднимают. Вначале испаряется азот (при температуре - 196  С), а затем и кислород (-183
С), а затем и кислород (-183  С), испаряясь, переходит в газообразное состояние.
С), испаряясь, переходит в газообразное состояние.
Свойства и применение кислорода

Рассмотрите картинки и поясните свои соображения. Какова причина длительного пребывания водолазов под водой? Где ещё используется кислородный баллон?
Физические свойства:
Кислород - это бесцветный газ без запаха и вкуса, относительно мало растворим в воде (при температуре 20°С в 100 объёмах воды растворяется 3,1 объёма кислорода). Кислород немного тяжелее воздуха, при температуре - 183 °С сжижается, а при понижении температуры до - 218,8 °С - затвердевает.
Химические свойства:
В обычных условиях кислород в чистом виде и в составе воздуха химически неактивен. Однако при нагревании его активность резко возрастает. Кислород может находиться во взаимодействии с большинством простых веществ - неметаллами и металлами, а также со сложными веществами.
Взаимодействие кислорода с неметаллами. Если раскалить под действием пламени спиртовки уголек в железной ложке, то он не загорится, а начнет дымиться. Поместим железную ложку с дымящимся угольком в банку с кислородом (для того, чтобы банка не разбилась, дно посыпаем мелким песком). Раскаленный уголек будет гореть без пламени, выделяя тепло. Если нальем в банку известковую воду 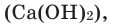 она помутнеет. Это свидетельствует о получении углекислого газа
она помутнеет. Это свидетельствует о получении углекислого газа 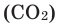 во время горения уголька. Полученный
во время горения уголька. Полученный 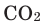 , вступая в реакцию с известковой водой, образует осадок белого цвета
, вступая в реакцию с известковой водой, образует осадок белого цвета 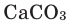 - карбонат кальция (известняк), который и приводит к помутнению известковой воды.
- карбонат кальция (известняк), который и приводит к помутнению известковой воды.
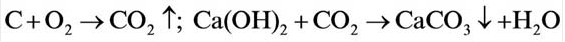
При горении раскаленного угля в условиях нехватки кислорода образуется очень опасный удушающий угарный газ:
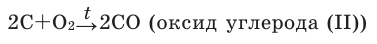
Нагреем в железной ложке немножко серы. Сера горит слабым голубоватым пламенем. Опустим ложку в банку с кислородом. Скорость горения серы увеличивается, появляется пламя ярко-голубого цвета. В банке образуется бесцветный газ с резким запахом - серный газ (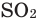 — оксид серы (IV). Эта реакция также является экзотермической - с выделением теплоты.
— оксид серы (IV). Эта реакция также является экзотермической - с выделением теплоты.
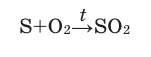
Возьмем немного фосфора в железной ложке и нагреем на огне спиртовки. Фосфор начинает гореть. Если опустить горящий фосфор в банку с кислородом, то горение ускорится и очень скоро банка наполнится белым дымом оксида фосфора (V). Горение фосфора тоже сопровождается выделением теплоты.
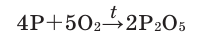
Все неметаллы, кроме фтора (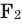 ), хлора (
), хлора (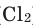 ), брома (
), брома (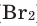 ), йода (
), йода ( 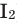 ), а из инертных газов - (Не, Ne, Ar, Кr, Хе), находятся в непосредственном взаимодействии с кислородом. Даже азот
), а из инертных газов - (Не, Ne, Ar, Кr, Хе), находятся в непосредственном взаимодействии с кислородом. Даже азот 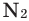 , обладающий очень устойчивой молекулой, при электрической искре образует с кислородом бесцветный газ (монооксид азота - NO), тем самым находясь с ним во взаимодействии. Однако эта реакция протекает с поглощением теплоты.
, обладающий очень устойчивой молекулой, при электрической искре образует с кислородом бесцветный газ (монооксид азота - NO), тем самым находясь с ним во взаимодействии. Однако эта реакция протекает с поглощением теплоты.
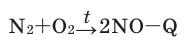
Взаимодействие кислорода с металлами. Кроме ценных (благородных) металлов (Ag, Au, Pt), большинство других металлов находятся в непосредственном взаимодействии с кислородом. Для вступления металлов в реакцию с кислородом, их следует нагреть, после чего реакция протекает самопроизвольно, с выделением света и тепла.
Магний горит в воздухе ярким, ослепительным пламенем. Если опустить ленту горящего магния в сосуд с кислородом, яркость пламени еще больше увеличится. В результате реакции образуется белый порошок оксида магния:
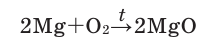
Если, насадив на железную проволоку деревянную щепку, мы зажжем ее и опустим в сосуд с кислородом, то вначале будет гореть кусок дерева, а затем железо. Железо горит без пламени, разбрасывая вокруг искры железной окалины.
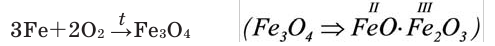
Сложные вещества, состоящие из двух элементов, один из которых является кислородом, называются оксидами.
Взаимодействие сложных веществ с кислородом. Как и простые вещества, сложные вещества тоже могут гореть в кислороде и окисляться. Реакции взаимодействия веществ с кислородом являются реакциями окисления. Ряд оксидов, взаимодействуя с кислородом, образуют новые оксиды.
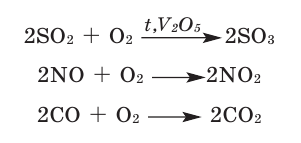
В наших квартирах ежедневно в газовых печах горит природный газ (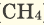 ), сопровождаясь выделением тепла (экзотермическая реакция) и образованием
), сопровождаясь выделением тепла (экзотермическая реакция) и образованием 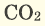 (углекислый газ) и
(углекислый газ) и 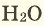 (вода).
(вода).
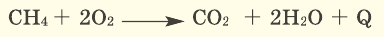
Серные соединения некоторых металлов (сульфиды) при горении в кислороде образуют два оксида.
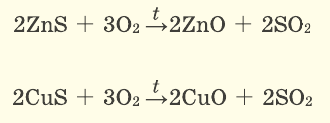
Применение:
Сварка и резка металлов происходит при участии чистого кислорода. В металлургической и химической промышленности больше всего используется кислород из воздуха. Например, при производстве чугуна и серной кислоты использование кислорода из воздуха позволяет значительно ускорить и повысить производительность производственных процессов.
В медицине чистый кислород применяют для облегчения затрудненного дыхания. В этих целях в больницах используются кислородные подушки и заполненные чистым кислородом стальные баллоны. Летающие на большой высоте летчики, космонавты, работающие под водой водолазы также пользуются небольшими по размеру кислородными баллонами.
Все живые организмы в природе при дыхании употребляют кислород, ежегодно усваивая миллионы тонн атмосферного кислорода. Так, например, было вычислено, что только люди употребляют в течение года свыше 1330 миллиардов кубических метров атмосферного кислорода. Кроме того, в громадных количествах атмосферный кислород тратится при сжигании топлива, на процессы гниения, при вулканических извержениях (рис. 1).
В организме человека и животных происходит медленное окисление глюкозы кислородом (рис. 2).

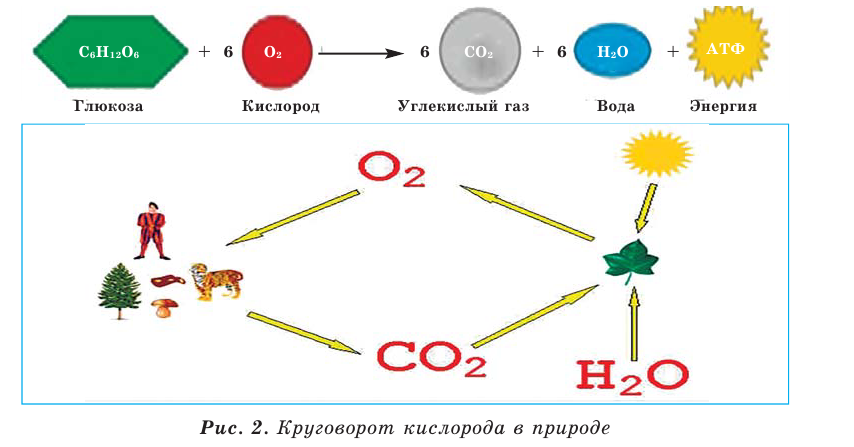
Кислород — химический элемент и простое вещество
В периодической системе элементов кислород О расположен во втором периоде в VIА-группе. Кроме него в эту группу входят еще три неметалла — сера S, селен Se и теллур Te, а также один металл — полоний Po.
Кислород в природе
Кислород составляет почти половину массы земной коры (49 %). Он входит в состав самых разнообразных соединений: воды, оксидов, солей и т. д. Этот элемент является неотъемлемой частью живой материи — тканей растений и животных.
Основным источником кислорода на Земле является атмосферный воздух, в котором на долю кислорода приходится около 21 % по объему. Несмотря на колоссальные масштабы потребления кислорода (процессы горения, дыхания, промышленные потребности и т. д.), содержание 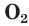 в атмосфере сохраняется постоянным благодаря жизнедеятельности зеленых растений. Круговорот кислорода в природе иллюстрирует рисунок 43.
в атмосфере сохраняется постоянным благодаря жизнедеятельности зеленых растений. Круговорот кислорода в природе иллюстрирует рисунок 43.
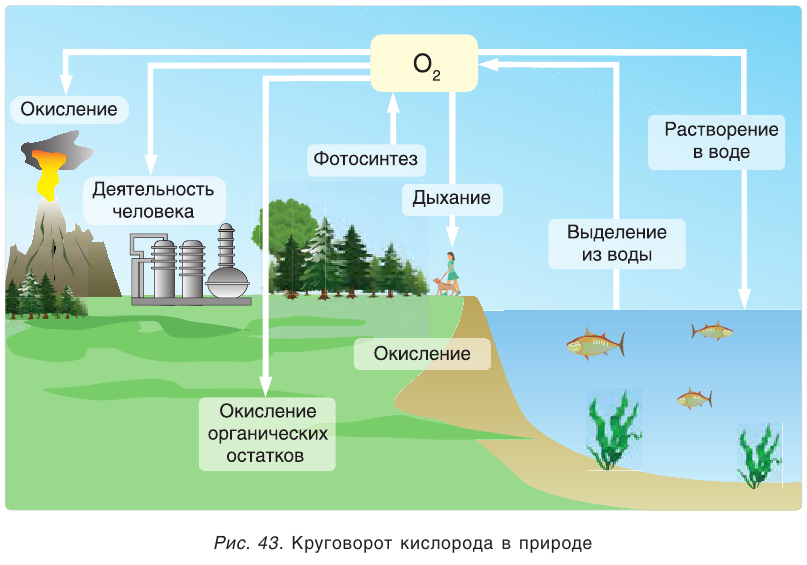
Процессы, происходящие в природе с участием кислорода, называются по-разному. Энергичное окисление с выделением тепла и света — горение, медленное окисление железа — ржавление, поглощение кислорода из воздуха живыми организмами — дыхание.
Строение атома кислорода
В атоме кислорода 8 электронов, которые располагаются на двух электронных слоях (рис. 44):
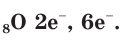
На внешнем электронном слое у атома кислорода находится 6 электронов, следовательно, до завершения этого слоя ему не хватает 2 электронов. Поэтому в своих
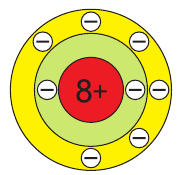

соединениях с металлами и водородом кислород обычно проявляет степень окисления, равную –2, как, например, в оксиде железа FeO. Кислород — второй по электроотрицательности химический элемент после фтора, поэтому только атомы фтора способны отнимать у него электроны. Положительную степень окисления +2 кислород проявляет только в соединении со фтором 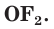 .
.
Строение и физические свойства простых веществ
С простым веществом кислородом вы уже познакомились в курсе химии 7-го класса. Напомним, что простое вещество кислород в природе существует в виде двух аллотропных модификаций — обычного кислорода 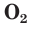 и озона
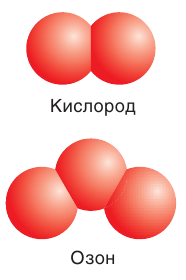
и озона 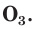 Разный состав, а следовательно, и разное строение молекул обуславливают и различные свойства этих веществ (рис. 45). Например, кислород
Разный состав, а следовательно, и разное строение молекул обуславливают и различные свойства этих веществ (рис. 45). Например, кислород 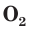 — газ без цвета и запаха, а озон
— газ без цвета и запаха, а озон 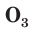 — газ светло-голубого цвета с резким характерным запахом. Они различаются также температурами плавления и кипения, реакционной способностью.
— газ светло-голубого цвета с резким характерным запахом. Они различаются также температурами плавления и кипения, реакционной способностью.
В природе озон образуется при грозовых разрядах и при окислении смолы хвойных деревьев. Небольшие количества озона в воздухе оказывают целебное действие на людей. Однако сильное обогащение воздуха озоном может стать опасным для здоровья. Увеличение содержания озона в воздухе выше предельно допустимой концентрации приводит к появлению головных болей, раздражению дыхательных путей и глаз, а затем к ослаблению сердечной деятельности. Источниками озона являются работающие приборы, в которых происходит высоковольтный электрический разряд — копировальные установки и лазерные принтеры, а также источники ультрафиолетового и рентгеновского излучения. Поэтому помещения, в которых находятся такие приборы, необходимо часто проветривать.

Озон сосредоточен в верхних слоях атмосферы, образуя озоновый слой, который защищает Землю и ее обитателей от жесткого ультрафиолетового излучения Солнца. Поверхности Земли достигают только те ультрафиолетовые лучи, которые не опасны для живых организмов. Когда мы загораем на солнце, на нашу кожу падают «мягкие» ультрафиолетовые лучи, не способные принести вреда здоровью (если загорать в меру).

Кислород и озон в воде мало растворимы. При 20 °С в 100 объемах 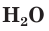 растворяется лишь около трех объемов
растворяется лишь около трех объемов 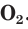 Благодаря этому в лаборатории кислород можно собирать методом вытеснения воды (рис. 46).
Благодаря этому в лаборатории кислород можно собирать методом вытеснения воды (рис. 46).
Химические свойства кислорода
Из-за высокой химической активности простое вещество кислород взаимодействует с большинством простых веществ и многими сложными веществами. Практически во всех своих реакциях кислород выступает в качестве окислителя.
Основными продуктами реакций кислорода с простыми веществами обычно являются оксиды. Окисление некоторых металлов происходит даже без нагревания, например:
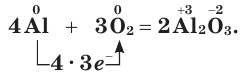
Но для протекания большинства реакций кислорода с металлами требуется нагревание, иногда значительное.
При окислении кислородом неметаллов обычно выделяется большое количество теплоты, как, например, при горении углерода и водорода:
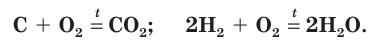
Кислород легко окисляет и многие сложные вещества. Например, известный вам из курса химии 7-го и 8-го классов оксид углерода(II) окисляется до углекислого газа:
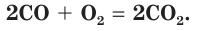
При окислении сульфида цинка образуются два оксида — оксид цинка и оксид серы(IV):
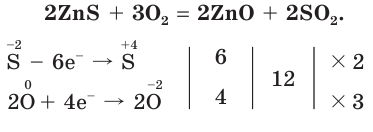
Окисляются кислородом и органические вещества, например метан:
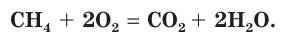
При этом, как правило, также образуются оксиды. Высокая окислительная способность кислорода является основой горения всех видов топлива.
С химическими свойствами озона вы познакомитесь в 11-м классе.
Применение кислорода и озона
Применение кислорода основано на его окислительных свойствах и свойстве поддерживать дыхание. Как окислитель он широко используется в металлургии, химической промышленности, других технологических процессах. Кислород применяют в качестве окислителя топлива в ракетных двигателях (рис. 47).

С участием кислорода совершается один из важнейших процессов жизнедеятельности живых организмов — дыхание. Окисление кислородом жиров, белков и углеводов служит источником энергии для живых организмов.
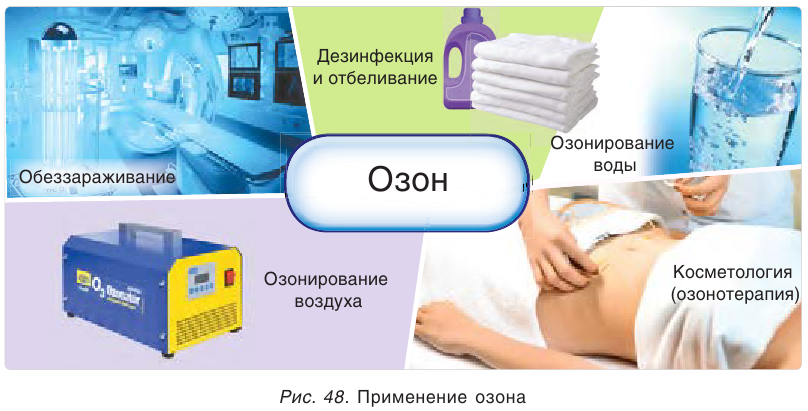
Озон используется для озонирования воздуха и питьевой воды, обезвреживания промышленных сточных вод, как дезинфицирующее средство в медицине, в качестве отбеливающего средства (рис. 48).
Атомы кислорода имеют на внешнем электронном слое по 6 электронов.
В соединениях с другими элементами кислород чаще всего проявляет степень окисления –2.
Известны две аллотропные модификации кислорода: кислород 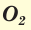 и озон
и озон 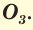
Кислород реагирует со многими простыми и сложными веществами.
Практически во всех реакциях кислород выступает в качестве окислителя.
| Рекомендую подробно изучить предметы: |
| Ещё лекции с примерами решения и объяснением: |