
Чистые вещества и смеси в химии - формулы и определение с примерами
Чистые вещества и смеси:
Человек постоянно встречает в жизни новые вещества и их смеси. Это объясняется тем, что в природе чистые вещества встречаются редко и большинство знакомых нам вещей являются смесью этих веществ.
Возьмите два химических стакана. В каждый из химических стаканов вначале влейте определённое количество воды. После этого в эти стаканы добавьте немного песка и сахара и размешайте. Что вы наблюдаете? Какова разница между исходными веществами и смесями, образовавшимися в химических стаканах? Как можно выделить из состава полученной смеси входящие в неё вещества?

В зависимости от постоянства физических свойств вещества делятся на 2 части (схема 1):
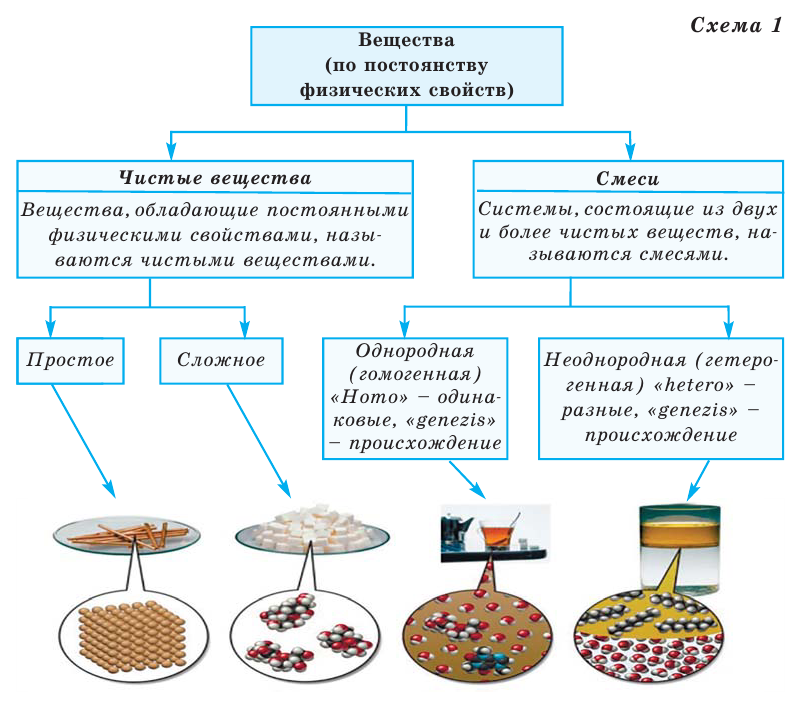
Чистые вещества обладают постоянными, а смеси — непостоянными физическими свойствами. Например, кислород при температуре - 182,9  С закипает, однако, так как в составе воздуха содержится смесь различных газов, температура его кипения непостоянна. Каждое чистое вещество обладает лишь присущими ему физическими свойствами и именно по этим свойствам его можно отличить от другого вещества: для уксусной кислоты - это запах, для поваренной соли - вкус, для меди - цвет и высокая электропроводность и т.д.
С закипает, однако, так как в составе воздуха содержится смесь различных газов, температура его кипения непостоянна. Каждое чистое вещество обладает лишь присущими ему физическими свойствами и именно по этим свойствам его можно отличить от другого вещества: для уксусной кислоты - это запах, для поваренной соли - вкус, для меди - цвет и высокая электропроводность и т.д.
Смеси бывают двух видов: однородные и неоднородные. Частицы веществ, составляющих однородные смеси, невозможно различить невооружённым глазом и даже под микроскопом. Например, смесь из поваренной соли и воды (рис. 1).
Частицы же веществ, составляющих неоднородные смеси, можно различить как простым глазом, так и при помощи микроскопа. Например, смесь из масла и воды. Однородные и неоднородные смеси можно разложить на составные части разными методами (схемы 2, 3).
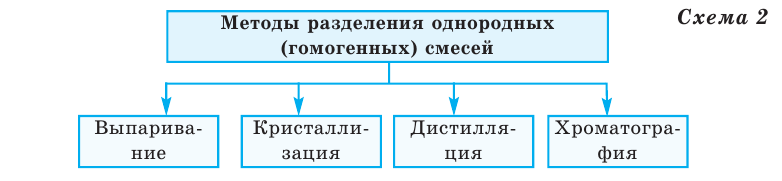
Выпаривание - данный метод применяется в тех случаях, когда твёрдое вещество находится в растворенном состоянии. Например, для выделения соли из солёной воды однородную смесь нагревают. В данном случае вода полностью выпаривается, а на дне посуды остаются белые кристаллики соли (рис. 2).

Выделение газов ( и др.) из их смеси с водой также происходит методом выпаривания. При этом из смеси в первую очередь выделяется газ.
и др.) из их смеси с водой также происходит методом выпаривания. При этом из смеси в первую очередь выделяется газ.
Кристаллизация - данный метод применяется в тех случаях, когда твёрдое вещество находится в жидкостях в растворённом состоянии. При таком методе воду из раствора выпаривают частично и полученный новый концентрированный раствор охлаждают. В таком случае выделяемое вещество оседает на дно в виде кристаллов. Путём кристаллизации получают более чистое вещество. Например, таким способом можно выделить сахар из его водного раствора.
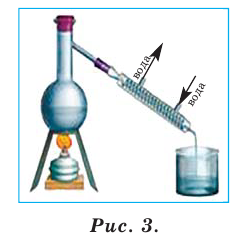
Дистилляция - данный метод применяется для выделения растворенных друг в друге веществ, обладающих разными температурами кипения (рис. 3). Метод дистилляции основан на различии в температурах кипения жидкостей в составе смеси. Например, этот метод можно использовать для разделения однородной смеси воды и этилового спирта. Потому что температуры кипения этих веществ разные. Вначале смесь нагревается. В таком случае в первую очередь выпаривается этиловый спирт, обладающий более низкой температурой кипения, т.е. закипающий при 78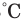 , и являющийся более летучей жидкостью. Выделяющиеся спиртовые пары, подвергаясь сжижению в холодильнике, собираются в посуду.
, и являющийся более летучей жидкостью. Выделяющиеся спиртовые пары, подвергаясь сжижению в холодильнике, собираются в посуду.
Хроматография — данный метод основан на способности адсорбции (поглощения) с различной скоростью отдельных веществ, составляющих смесь, на поверхности другого вещества и их десорбции (выделения). При помощи метода хроматографии можно разделить однородные жидкие смеси и смеси газов на составные части (рис. 4).

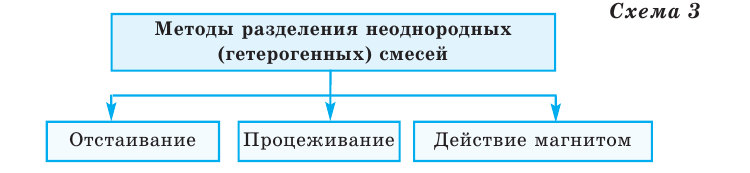
Отстаивание - этот метод основан на различии плотностей жидкостей. Данный метод можно использовать в двух случаях:
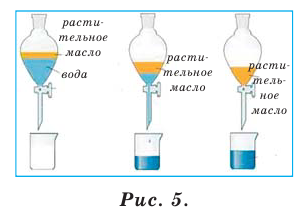
а) при разделении нерастворимых друг в друге жидких веществ с разными плотностями. Для этого пользуются делительной воронкой. Например, выделение растительного масла из его смеси с водой, сливок из молока и др. (рис. 5).
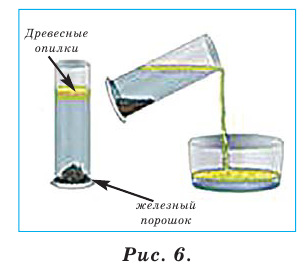
б) при разделении посредством воды двух не растворяющихся в воде твёрдых веществ с разными плотностями. Например, смесь из железного порошка и древесных опилок можно разделить, добавив в эту смесь воду (рис. 6). Вещество с малой плотностью всплывёт на поверхность, а вещество с более высокой плотностью осядет на дно.
Процеживание (фильтрация) - данный метод используется для отделения нерастворимых в воде твёрдых веществ. Например,
песок + вода, сера + вода, железный порошок + вода, глина + вода, известняк + вода, древесные опилки + вода.
При процеживании (фильтрации) используют фильтровальную бумагу. Во время процеживания смеси твёрдое вещество остаётся на поверхности фильтровальной бумаги (рис.7). Данным методом можно разделить смесь из двух разных веществ, одно из которых растворяется, а другое - не растворяется в воде. Например, для разделения смеси из соли и песка, в эту смесь вначале добавляют воду и размешивают, а затем полученную новую смесь процеживают через фильтровальную бумагу. Во время процеживания песок остаётся на поверхности фильтровальной бумаги, а солёная вода проходит через неё.

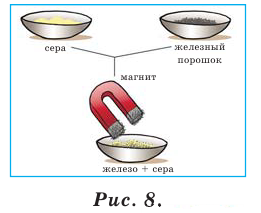
Воздействие магнитом - этим методом пользуются для отделения железа из его смеси с твёрдыми веществами (рис. 8). Например, железный порошок+серный порошок, железный порошок + древесные опилки, железный порошок + песок. Путём воздействия магнитом можно разделить эти смеси на составные части. В этом случае железный порошок притягивается магнитом, а другое вещество - нет.
Такие смеси, как глина + вода, песок + вода, мел + вода, можно разделить также методом осаждения. Смесь оставляется на некоторое время в нетронутом виде, нерастворимое в воде вещество оседает на дно.
| Рекомендую подробно изучить предметы: |
| Ещё лекции с примерами решения и объяснением: |